为何你的动物实验总失败?很可能是剂量没算对:一份科学给药指南
实验动物作为人类的“替身”,在科学研究中具有悠久的历史。早在古代,动物已被用于生理机制的初步探索;至17世纪,威廉·哈维通过动物实验揭示血液循环规律,为现代医学奠定重要基础。随着20世纪遗传学与微生物控制理论的发展,实验动物学逐渐成为一门独立学科,并于20世纪50年代建立起标准化体系。
在众多实验动物中,小鼠因其基因组与人类高度同源、遗传背景清晰等优势,成为应用最广泛的模式动物。除了小鼠,大鼠、兔、犬以及与人类遗传背景更为接近的灵长类动物,也被广泛应用于生物医药研究。选择合适的动物模型当然很重要,精准的给药剂量设计也是确保实验科学性与可重复性的关键环节。剂量过低可能导致药效无法充分显现,而剂量过高则可能引发毒性反应或干扰对药效机制的正确判断。因此,合理计算并优化给药策略,已成为衔接临床前研究与临床转化的重要桥梁。
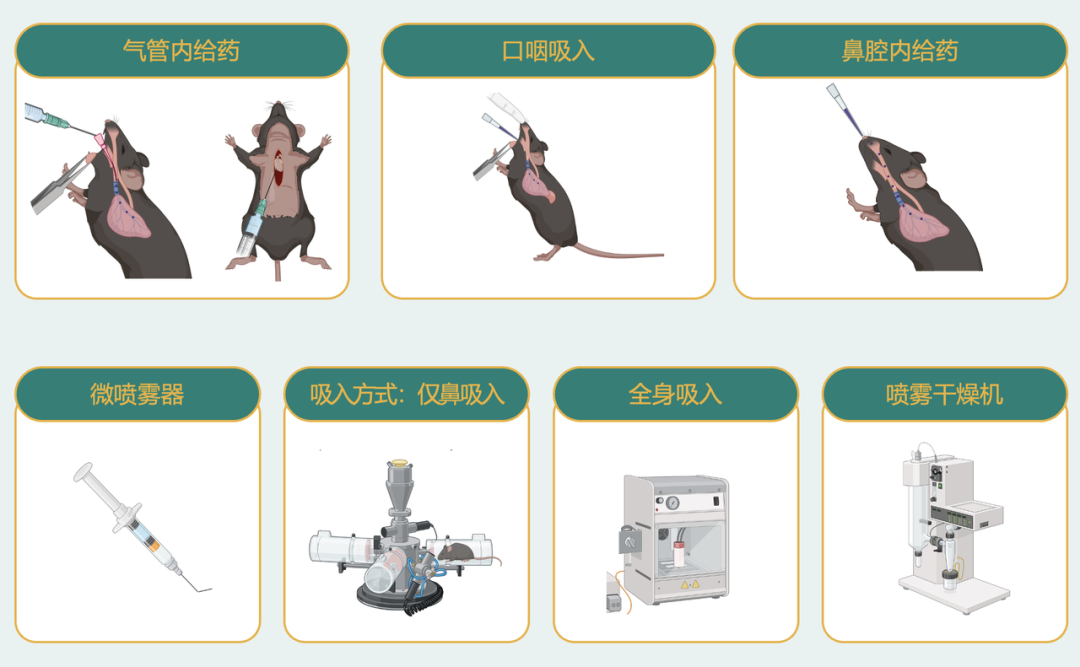
图1. 集萃药康呼吸系统平台给药方式
给药剂量计算:从基础公式到精准换算
基础计算原则
给药剂量指单位体重所给予的药物量,常以mg/kg或g/kg表示。药物的药效和毒性多呈剂量依赖性,而达到相同药效的剂量因动物种属、年龄及给药途径有所不同。
其基本计算公式为:给药量(mg/kg)= 药物剂量(mg)/ 动物体重(kg)。
例如,药物剂量为10 mg,小鼠体重为20 g(0.02 kg),则给药量为:10 mg / 0.02 kg = 500 mg/kg。
体表面积换算:更为科学的方法
在动物体重差异较大时,采用体表面积剂量(mg/m²)是更准确的方法。该法基于能量代谢原理,即动物与人体释放的能量与体表面积成正比。多项研究表明,基础代谢率、热能消耗、肝肾功能、血药浓度等指标均与体表面积密切相关。
体表面积计算公式常采用:BSA(m²)=[K × W^(2/3)]/10000,其中K为体型常数,W为体重(g),10000 是 cm² → m² 的换算系数。
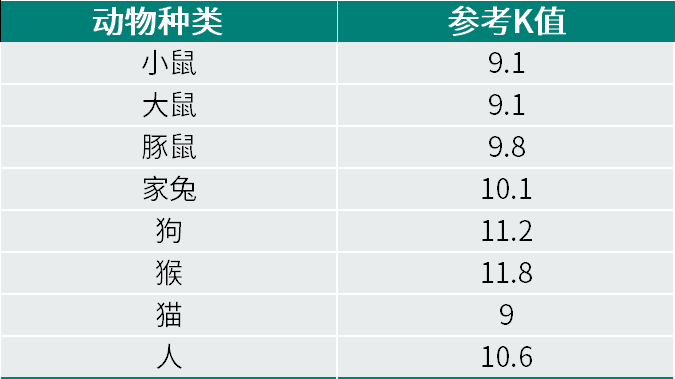
表1. 常见动物的参考K值[1]
体表面积归一化因子(Km)是药物剂量跨物种科学换算的关键参数,其核心依据为剂量应与体表面积成正比,而非体重,这一方法被美国FDA和欧洲EMA推荐为标准剂量换算依据。
借助Km值,可实现从动物剂量到人类等效剂量(HED)或从人类剂量到动物等效剂量(AED)的互相换算[2]:从动物剂量换算为人类等效剂量(HED):HED (mg/kg)=动物剂量 (mg/kg) × (动物 Km/人类 Km);
从人类剂量换算为动物等效剂量(AED):AED (mg/kg)=人类剂量 (mg/kg) × (人类 Km/动物 Km)。
也可借助剂量换算系数直接折算:从动物剂量换算为人类等效剂量(HED):HED (mg/kg)=动物剂量 (mg/kg) ÷ 剂量换算系数;
从人类剂量换算为动物等效剂量(AED):AED (mg/kg)=人类剂量 (mg/kg) × 剂量换算系数。
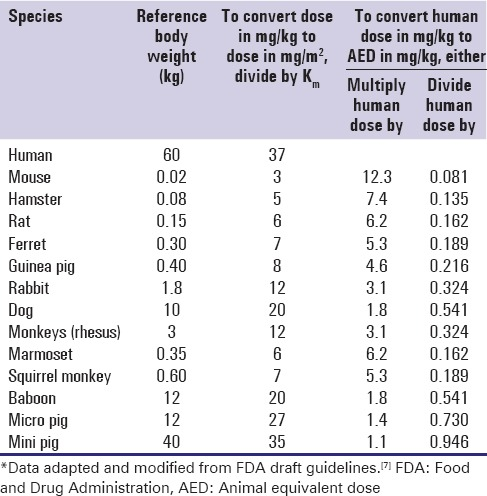
表2. 常见物种Km值与剂量换算系数[2]
实际换算示例
假设某药物的人类临床剂量为100 mg(按70 kg体重),需换算为200 g大鼠的剂量(mg/kg)。
利用Km值进行计算
大鼠剂量(mg/kg) = 人类剂量 (mg/kg) × (人类 Km/大鼠Km) = 100/70 × (37/6) ≈ 9 (mg/kg)。
折算系数法
已知大鼠剂量约为人类剂量的6.2倍,因此大鼠剂量 = 6.2 ×(100 / 70)≈ 9 mg/kg。
不同给药途径的技术要点和剂量调整
常用给药途径及其特点
不同给药途径影响药物的吸收途径、速率、分布范围及代谢方式,进而影响药效表现及毒性。
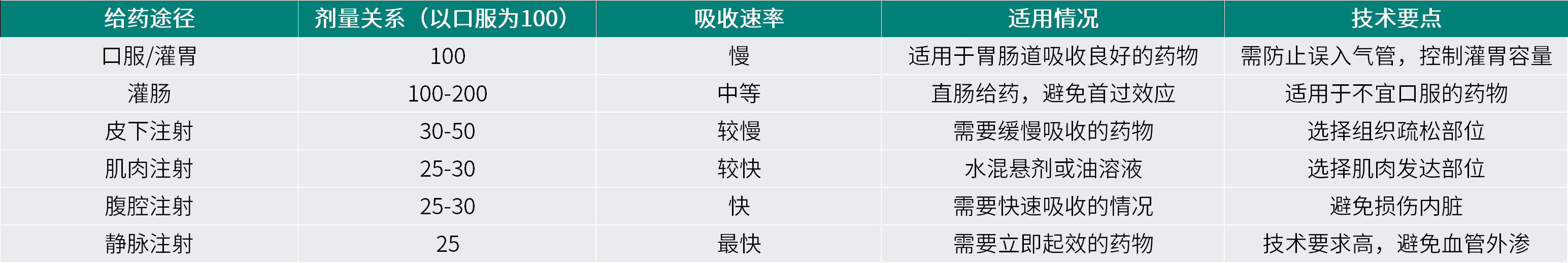
表3. 不同给药途径的剂量关系及特点[3]
最大给药容量的控制
为确保动物健康并准确评估药效,需严格控制每次给药的最大容量。一般原则如下:
静脉注射量宜小于体重的1/100;
皮下、肌内及腹腔注射容量不宜超过体重的 1/40[3];
例如,对一只20 g小鼠,腹腔注射不宜超过0.5ml,静脉注射不宜超过0.2ml。
从文献到实践:给药剂量的优化策略
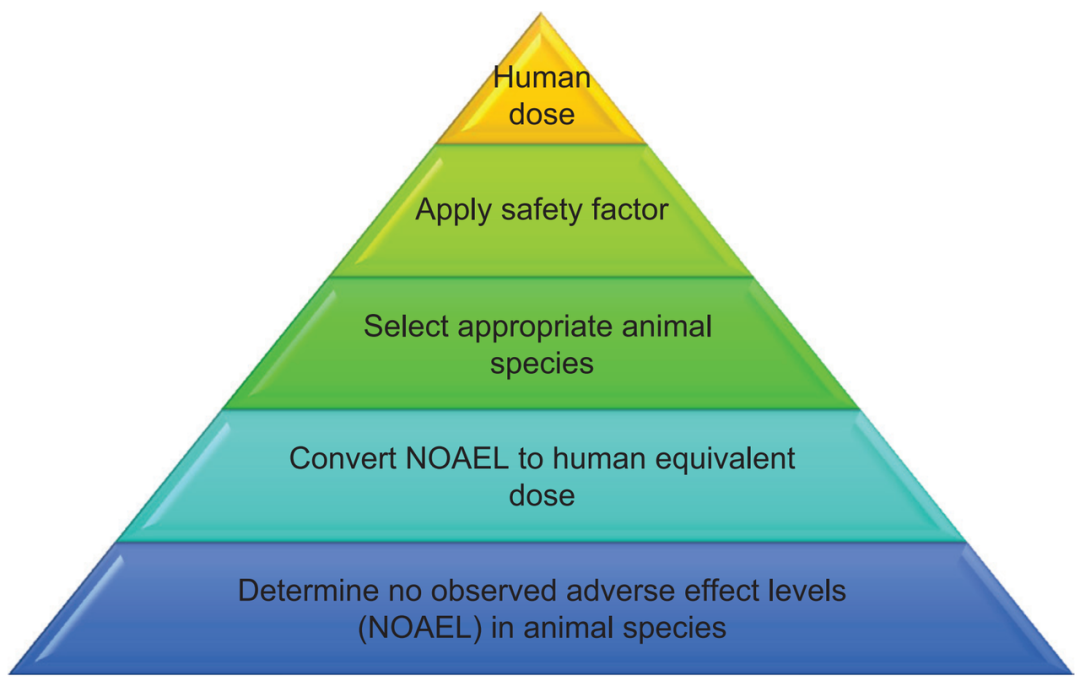
图2. 科学研究中估算起始剂量的五个步骤[2]
文献查询与剂量确定
确定剂量的首要步骤是系统检索相关文献。例如,在研究LY294002在BALB/c小鼠乳腺癌模型中的剂量时,可检索:“LY294002 breast tumor BALB/c mg/kg”或“LY294002 breast cancer BALB/c mg/kg”。如无直接文献参考,可采取如下策略:
汇总相近动物的给药数据;
利用物种间剂量换算公式:动物B剂量 = 动物A剂量 ×(动物A Km / 动物B Km)。
对全新化合物,通常先进行急性毒性实验,测定其半数致死量(LD₅₀)或最大耐受剂量(MTD),并以1/10–1/5 MTD 作为初始给药剂量。具体步骤包括:
若首次实验无明显效果且无中毒,可增加剂量;
若出现中毒但药效显著,则应降低剂量;
推荐设置多剂量组,以全面评估药物效果。
特殊情况的剂量调整
年龄因素:幼龄动物代谢系统尚未成熟,对药物更敏感,剂量应低于成年动物;
药物特性:需综合考虑生物利用度、半衰期、峰值浓度等参数;
溶剂选择:不同溶剂可能影响药物吸收与生物利用度。
种属差异性的考量
不同动物对同一药物的反应存在种属差异,与代谢途径及速率密切相关,因此,不宜完全照搬等效剂量,应一半依据计算,一半依靠实验验证。例如:
犬无汗腺,对发汗药不敏感,对流涎药敏感;
大鼠无胆囊,利胆药及肝肠循环明显的药物表现不同;
吗啡对多数动物有抑制作用,但对猫却引起兴奋。
在创新药物研发过程中,选择恰当的实验动物模型并制定科学的给药方案是至关重要的环节。集萃药康依托丰富的小鼠模型资源、专业的技术支持以及全面的数据分析能力,为客户提供高质量的临床前研究解决方案。无论您致力于小分子药物、抗体药物、核酸药物,还是细胞与基因治疗领域的研究,集萃药康均能提供精准匹配的模型资源与专业技术服务,助力研发进程高效推进。
参考文献
[1] 宁夏医科大学实验动物中心https://www.nxmu.edu.cn/sydwzx/info/1015/1211.htm
[2] J Basic Clin Pharm. 2016 Mar;7(2):27–31.
[3]《医学动物实验技术》.魏泓主编, 2024.
[4] Estimating the Maximum Safe Starting Dose in Initial Clinical Trials for Therapeutics in Adult Healthy Volunteers. FDA, 2005.

