精准免疫杀伤:抗体药物ADCC/ADCP/CDC机制全解析与体外评价平台实战
抗体药物通过调节免疫功能发挥抗肿瘤作用,最核心的机制是借助与肿瘤细胞表面抗原的特异性结合,在免疫细胞协同下实现对肿瘤细胞的精准杀伤。这一过程中,抗体Fc端主要依赖ADCC、ADCP和CDC三种关键效应,它们共同构成抗体介导的抗肿瘤免疫网络。
ADCC(Antibody-Dependent Cell-mediated Cytotoxicity)
即抗体依赖的细胞介导的细胞毒性作用。当抗体的Fab段与肿瘤细胞或病毒感染细胞表面的抗原表位结合后,其Fc段会与NK细胞、巨噬细胞等杀伤细胞表面的Fc受体(FcR)特异性结合,通过这种“桥接”作用激活杀伤细胞,直接启动对靶细胞的杀伤程序。
ADCP(Antibody-Dependent Cellular Phagocytosis)
即抗体依赖性细胞介导的吞噬作用。抗体与肿瘤细胞表面抗原结合后,其Fc段可与巨噬细胞等效应细胞表面Fcγ受体(如 FcγRIII/CD16A、FcγRII/CD32A、FcγRI/CD64)结合,触发巨噬细胞的吞噬信号,显著增强对肿瘤细胞的吞噬清除能力。
CDC(Complement Dependent Cytotoxicity)
即补体依赖的细胞毒性作用。抗体与肿瘤细胞表面抗原结合形成复合物后,会招募补体蛋白 C1q并激活补体系统经典途径。经一系列级联反应,最终形成攻膜复合体(MAC),该复合体可直接插入肿瘤细胞膜,导致细胞裂解并诱导凋亡,实现对肿瘤细胞的杀伤。
这些机制相互协同,通过抗体的靶向性与免疫系统的效应功能联动,成为抗体药物发挥抗肿瘤活性的核心基础。
案例分享1 利妥昔单抗(Rituximab)的 ADCC 活性检测
目的:Raji是一株天然表达CD20的人淋巴瘤细胞系,使用PBMC作为效应细胞,检测Rituximab对肿瘤细胞的ADCC效应。
结果:Rituximab特异性靶向杀伤表达 CD20的Raji肿瘤细胞,且杀伤能力呈显著剂量依赖性增强。
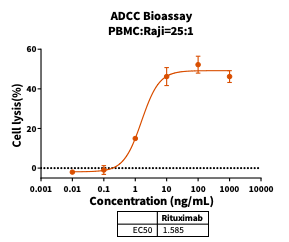
图1. Rituximab的 ADCC 活性检测
案例分享2 Rituximab的ADCP 活性检测
目的:使用体外诱导的单核来源巨噬细胞,通过流式细胞术评估Rituximab对Raji细胞的ADCP效应。
结果:Rituximab可有效激活单核来源巨噬细胞的ADCP效应,显著增强对Raji细胞的吞噬能力。
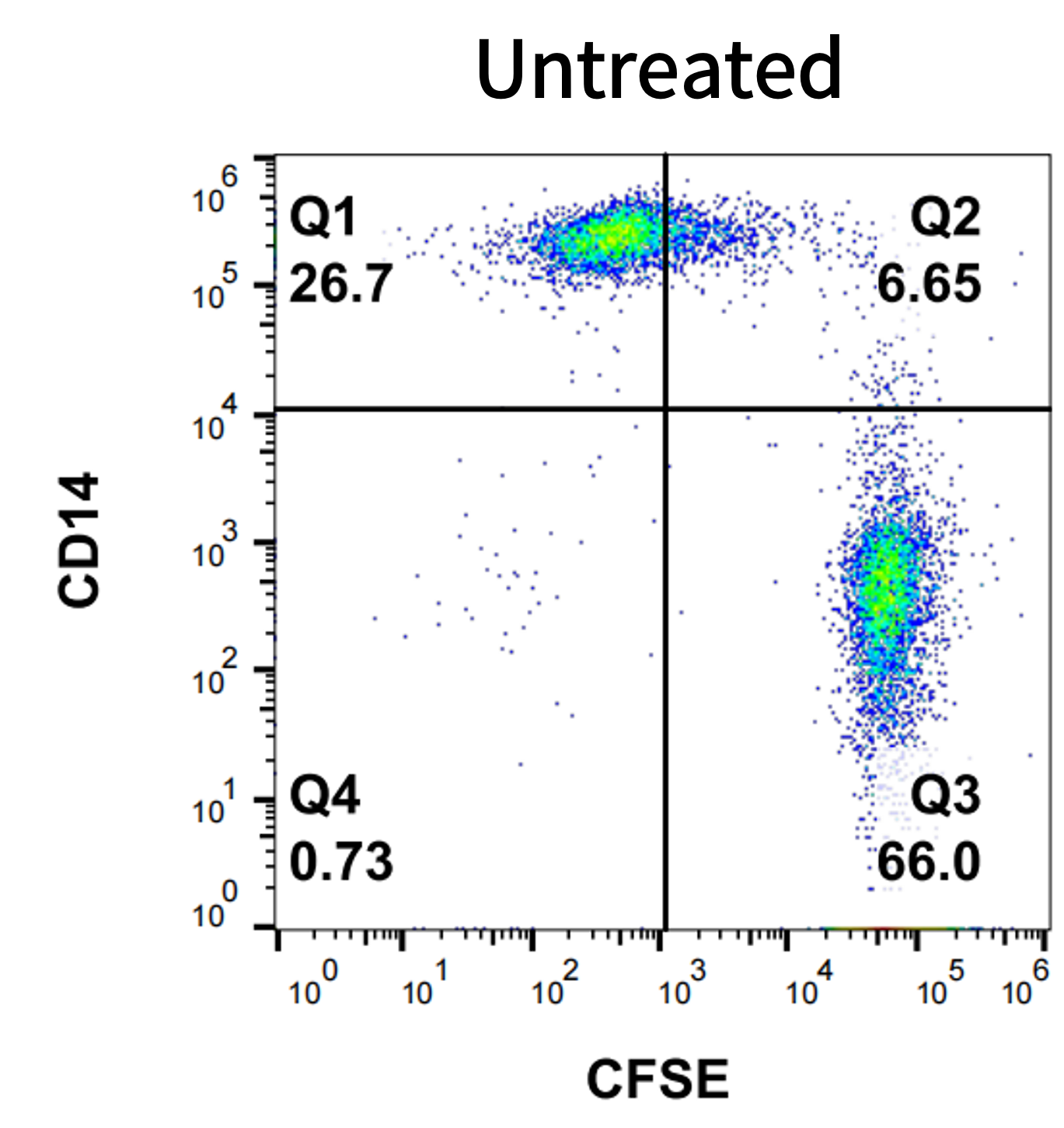
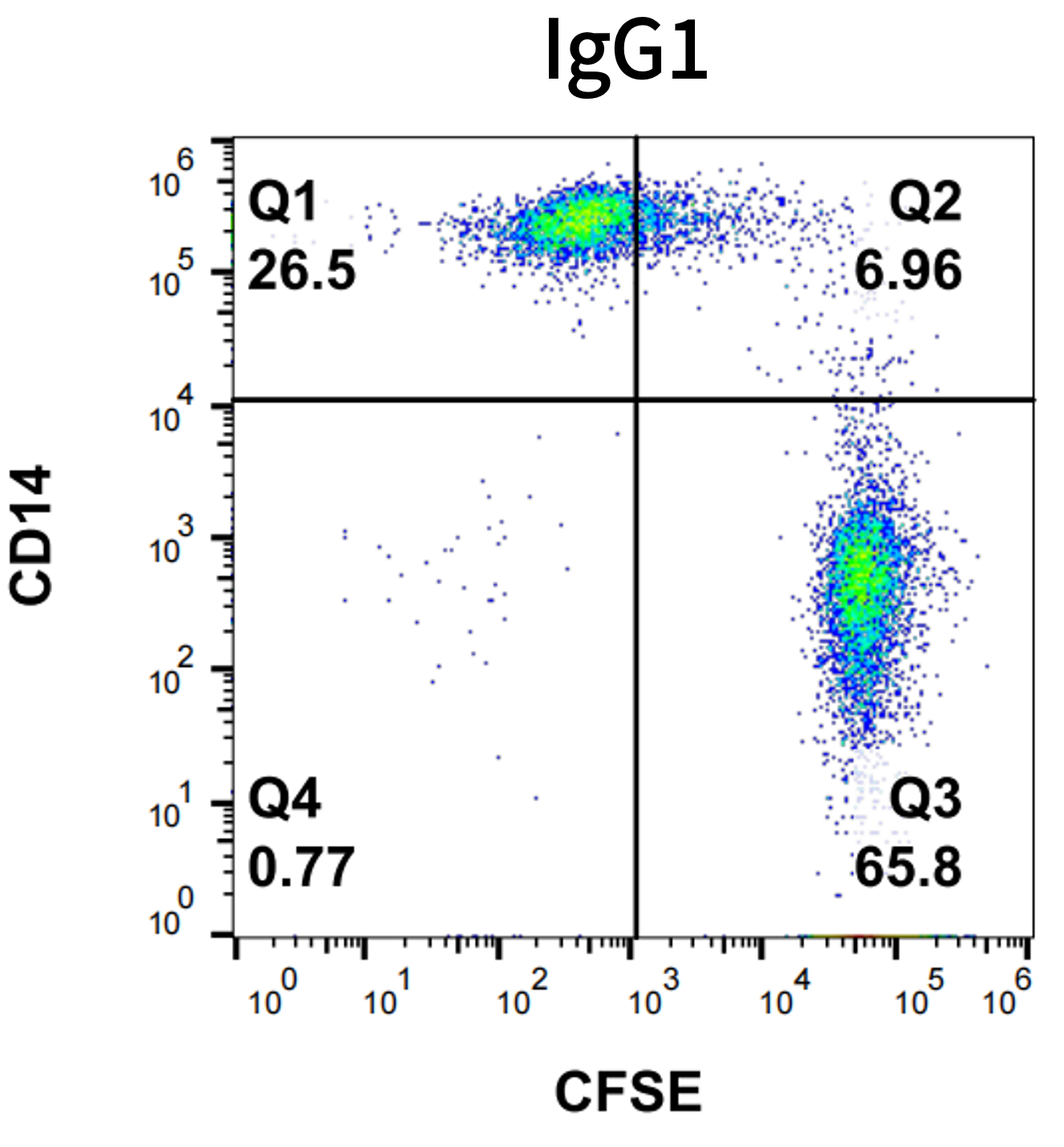
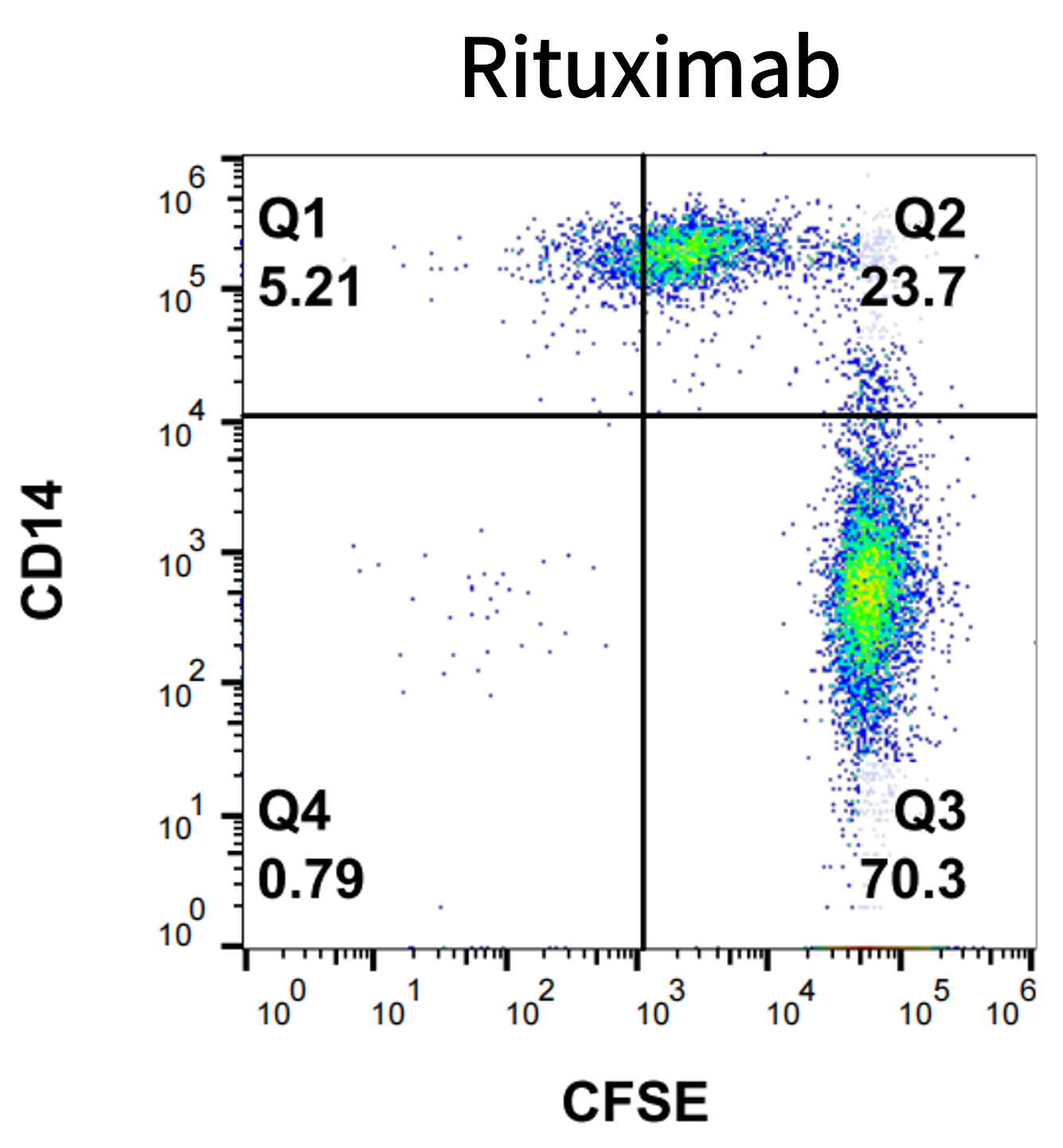
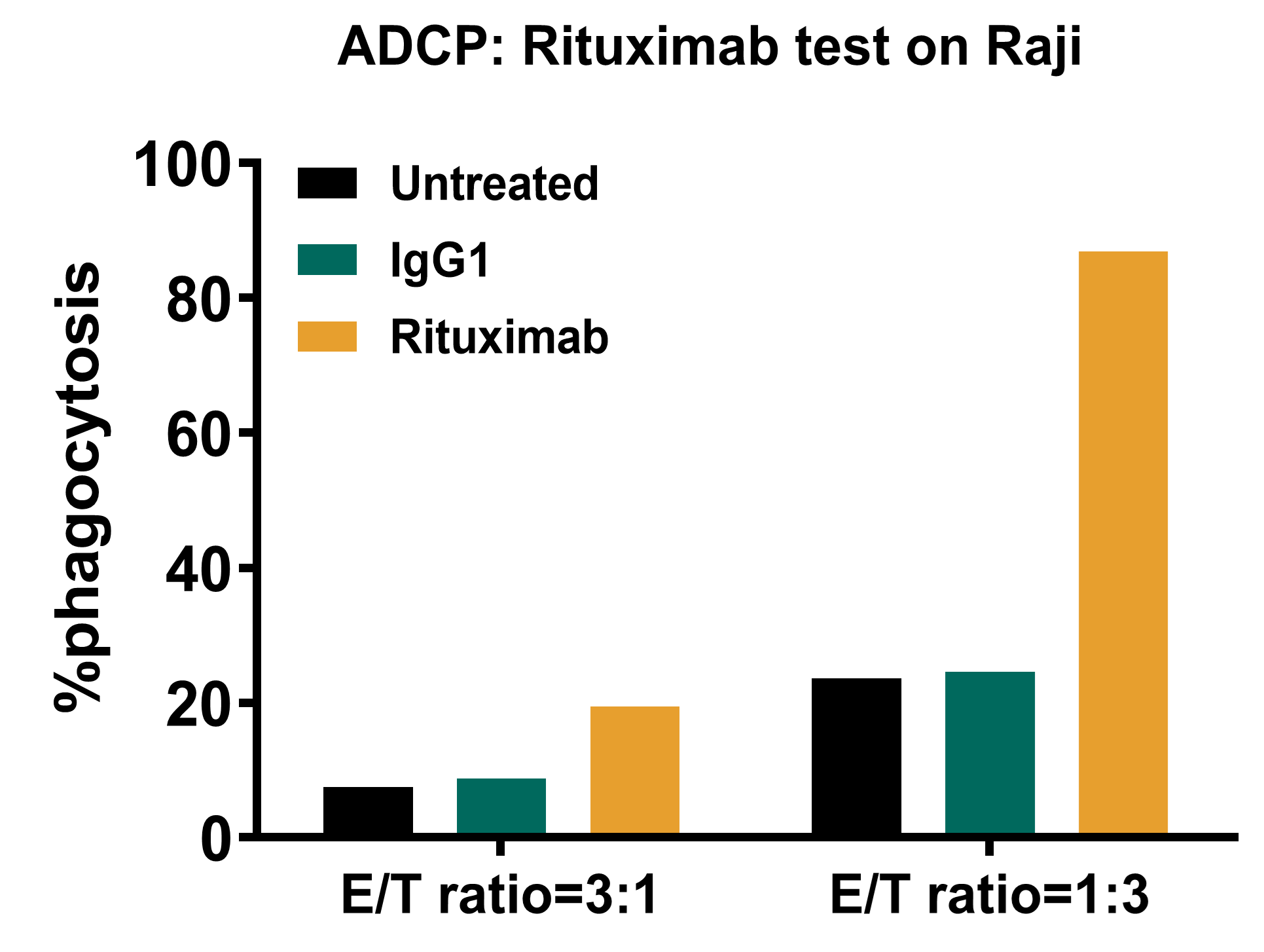
图2. Rituximab的ADCP活性检测
案例分享3 Rituximab的CDC 活性检测
目的:评估Rituximab通过CDC作用杀伤 Raji细胞的效果。
结果:Rituximab可经CDC作用杀伤Raji细胞,且效果与浓度相关。
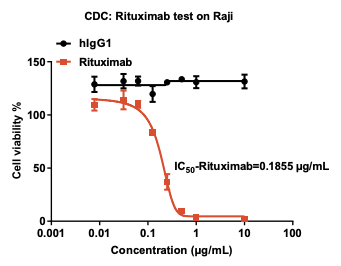
图3. Rituximab的CDC活性检测
案例分享4 评价人和小鼠来源NK细胞的ADCC效应
目的:以PBMC分离的人源NK细胞、huHSC-NCG-hIL2小鼠脾脏分离的鼠源NK 细胞为效应细胞,评估Trastuzumab、Margetuximab对人乳腺癌JIMT-1细胞的ADCC能力,对比人 / 鼠源NK细胞在药物评价中的应用效果。
结果:huHSC-NCG-hIL2小鼠来源NK细胞可在体外稳定复现ADCC药物Trastuzumab 的剂量依赖效应,数据趋势与人PBMC分离的NK细胞(human PBNK)高度一致;同时,能精准区分Trastuzumab与其ADCC增强型改造药物Margetuximab的药效差异。
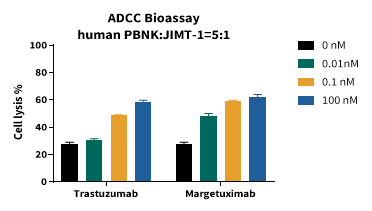
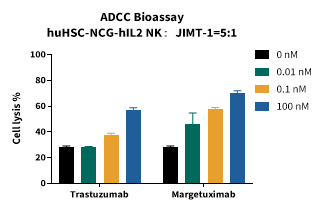
图4. 人和小鼠来源NK细胞的ADCC效应
案例分享5 报告基因法检测Rituximab的 ADCC与ADCP活性
目的:使用工程化改造的Jurkat-NFAT-CD16a和Jurkat-NFAT-CD32a报告基因细胞系作为效应细胞,验证Rituximab的 ADCC与ADCP活性。
结果:仅在存在肿瘤细胞的实验组中,Rituximab可
活NFAT通路,分别体现出ADCC与ADCP活性。
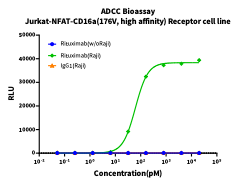
图5. 报告基因法检测Rituximab的 ADCC 与 ADCP 活性效应
集萃药康(GemPharmatech)建立了完善的免疫相关细胞杀伤功能评价平台,可系统开展ADCC、ADCP和CDC的全方位评估,为候选药物的筛选与优化提供强有力的技术支持,提升临床前研究成功率。

