从血液瘤到实体瘤:TCE技术进展及药康生物一站式临床前解决方案
背景与机制优势
肿瘤免疫治疗与细胞治疗在多种肿瘤中取得突破,但在MHC分子下调或免疫浸润不足的实体瘤中疗效有限。自体CAR-T疗法受限于定制周期长、成本高、制备流程复杂。
TCE(T细胞衔接器)作为标准化即用型蛋白药物,具备开发周期短、生产放大可控、质量一致性高等优势,有利于规模化临床应用。
TCE通过直接桥接T细胞与肿瘤细胞,高效募集并激活内源性T细胞,不依赖MHC抗原呈递,在免疫抑制性肿瘤微环境中具有机制优势。
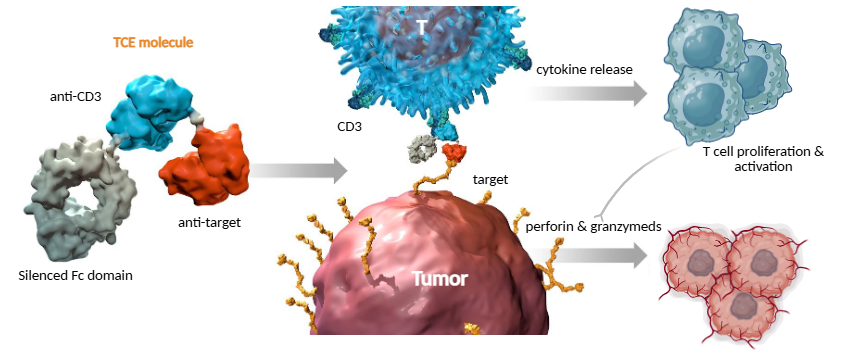
图1. TCE药物作用机制
上市与临床进展
全球已有11款TCE药物获批上市。
Tarlatamab-dlle为首款针对小细胞肺癌(SCLC)的药物,标志着TCE从血液肿瘤扩展至实体瘤。
实体瘤适应症方面,SCLC和转移性去势抵抗性前列腺癌(mCRPC)进展最快,主流靶点包括DLL3、STEAP1、PSMA,多项III期研究推进中。
研发挑战与优化方向
向实体瘤规模化应用面临肿瘤穿透性差、抗原异质性、半衰期短、CRS风险及脱靶毒性等问题。
研发热点聚焦于:
高特异性靶点挖掘
TCR融合拓展胞内抗原
CD3亲和力调控与条件激活设计以降低CRS风险
半衰期优化
联合免疫/化疗
mRNA局部递送突破肿瘤微环境限制
药康生物临床前评价解决方案
非临床药效评价对模型选择、人源化程度、供体差异、药效窗口及药物毒性等提出高要求。
体外药物评价
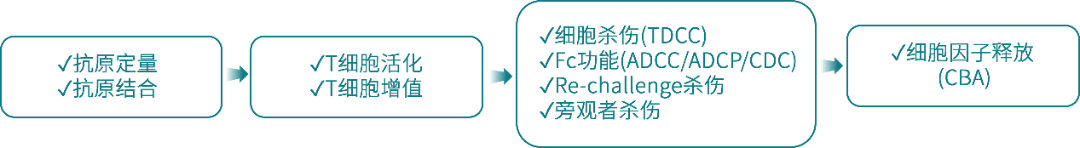
已建立系统化体外药效评价体系,涵盖靶点结合、T细胞功能及体外杀伤,形成标准化评价流程。
体内药物评价
基于自主研发的NCG及NCG-MHC-dKO模型,建立多种适应症的PBMC荷瘤药效评价体系,储备200多批次高适用性PBMC供体。
通过定期构建HSC重建模型,建立基于HSC的TCE药物评价体系,满足长周期评价及non-GLP安全性评价需求。
拥有双背景hCD3人源化小鼠,适配190多个靶点的人源化改造鼠源细胞,积累丰富药效数据及机制研究经验。
构建30多种CD3与TAA双人源化小鼠,支持TCE安全性评价研究。
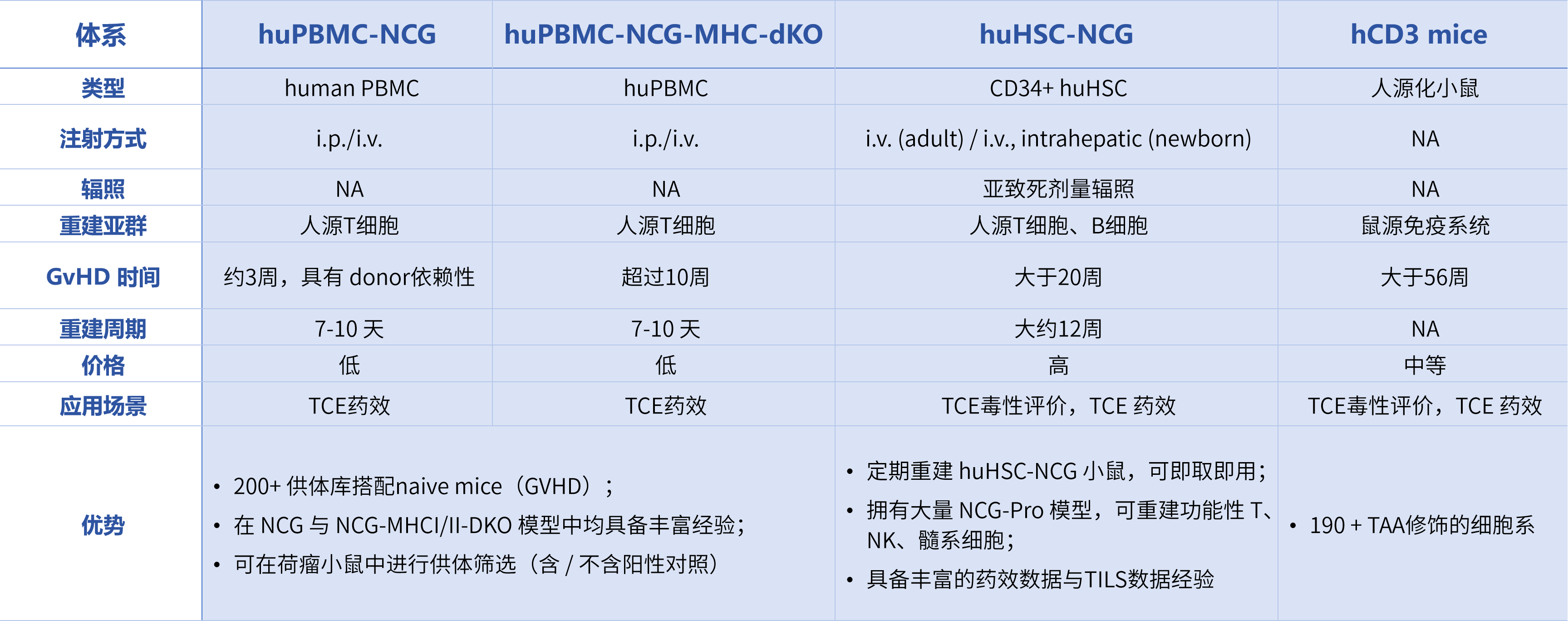
图2. 根据待测药物MOA及肿瘤特性选择最优方案
案例分享:Xaluritamig(CD3-STEAP1)药效评价
体外实验:Xaluritamig可有效发挥T细胞依赖性细胞毒性(TDCC)作用。
体内实验:对STEAP1高表达的LNCaP clone FGC细胞系以及STEAP1低表达的22RV1细胞系,均表现出显著肿瘤生长抑制效果。
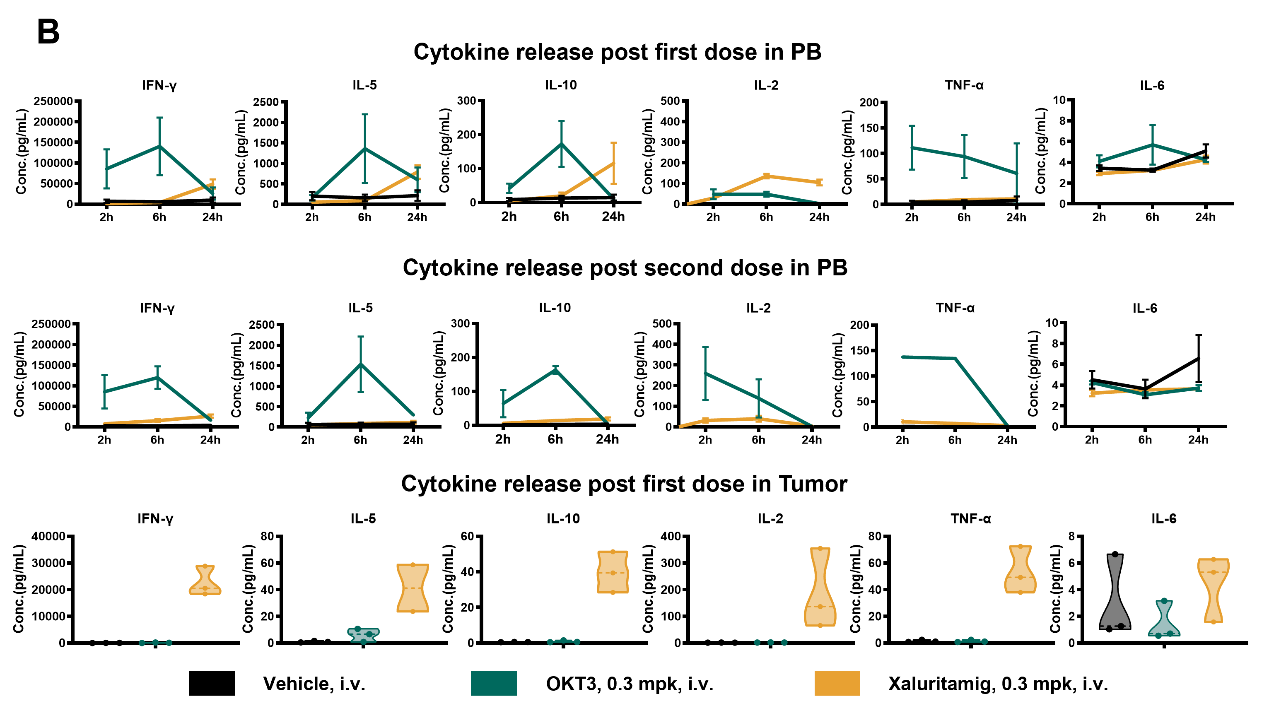
Xaluritamig能够有效激活系统性抗肿瘤免疫应答,并在肿瘤局部特异性引发免疫反应。
该药物诱发细胞因子释放综合征(CRS)的风险较低。
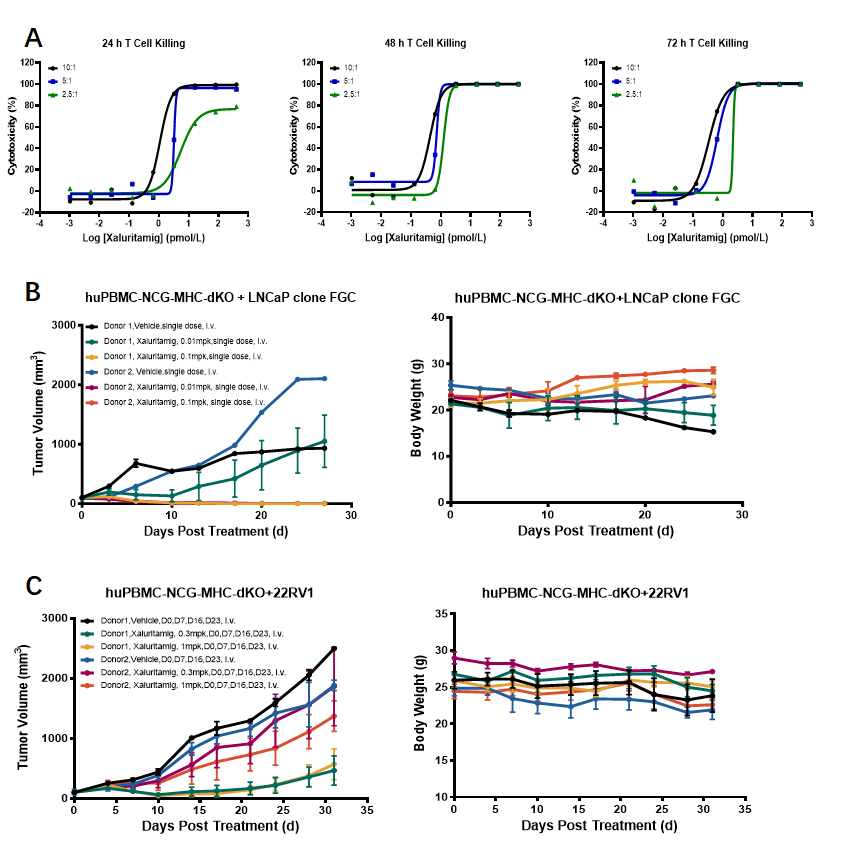
图3. Xaluritamig体外及体内药效评价
图4. 体外及体内Xaluritamig 诱导的细胞因子释放
总结
TCE药物具有精准靶向、强效激活T细胞、杀伤效率高、给药便捷、研发与生产成本相对较低的特点,临床转化潜力突出,在血液肿瘤与实体瘤中均有广阔应用前景。
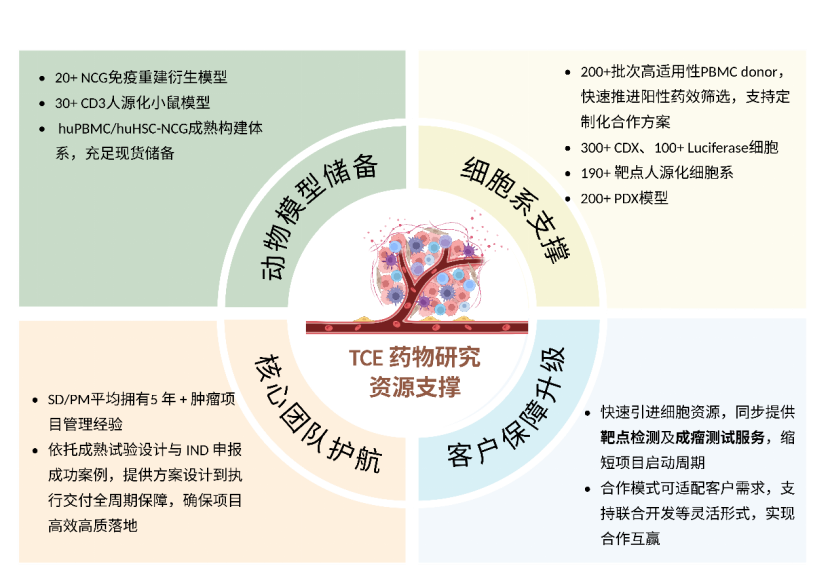
药康生物提供从体外评价到体内药理药效、非临床毒理研究的全链条整合服务,覆盖TCE药物研发关键环节,为有效性、安全性评价提供系统、可靠的非临床评价载体。