拒绝翻车!BKS-DB与DIO小鼠模型操作全指南
在代谢疾病研究中,BKS-DB(糖尿病模型)与DIO(饮食诱导肥胖模型)小鼠的应用需遵循规范的操作流程。本文系统梳理两类模型的核心特征、饲养管理及实验操作的关键环节。
一、BKS-DB小鼠:糖尿病与糖尿病肾病模型
1. 模型特征
血糖代谢稳定:无需外源诱导,可自发呈现持续性高血糖,模拟人类2型糖尿病的血糖调节紊乱。
病理表型全面:自发肥胖、高血糖、高胰岛素血症及胰岛素抵抗,并伴随糖尿病肾病、视网膜病变等并发症,病理进程与人类疾病高度相似。
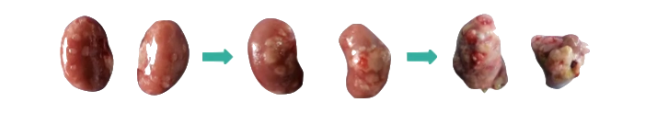
图1. 糖肾解剖表型示例
2. 饲养管理要点
接收后管理
SPF级环境饲养,病原体感染可延迟或阻碍糖尿病发生。
确保充足食物与饮水(肥胖小鼠获取食物和水的难度增加)。
到达后至少适应1周再进行实验。
适当降低饲养密度。
并发症预防与处理
环境优化:状态不佳时每周至少换笼3次,保持干燥卫生;勤换垫料;清除笼内尖锐物。
皮肤护理:出现皮肤破损时,用碘伏消毒并保持干燥。如需注射给药,选用细针头,分散注射点,并加强术后观察。
腹泻/便秘:加强观察,及时清洁肛周。必要时辅助便秘小鼠排便。
严重情况:皮肤破溃严重、持续性腹泻或体重持续下降时,应及时实施安乐死。
3. 血糖检测规范
随机血糖检测
检测前校准血糖仪,确认试纸有效。
固定小鼠避免过度应激,酒精消毒尾尖,待酒精挥发后采血。
使用第二滴血进行检测,避免组织液混入。
记录检测时间与结果。建议在早晨进行,保持同一批实验检测时间一致。
禁食血糖检测
白天禁食5小时(不禁水),检测后立即恢复饮食。
禁食时间不宜超过6小时。
采血方式保持一致。
二、DIO小鼠:饮食诱导肥胖模型
1. 模型特征
通过高脂饮食诱导形成肥胖表型,伴随胰岛素抵抗、血脂异常等代谢改变,模拟人类因饮食结构不当引发的肥胖及相关代谢异常。
与基因编辑肥胖模型相比,其临床模拟性更好,造模成功率较高。
2. 造模注意事项
严格防止对照组与模型组饲料串混,可采取单独笼养。
造模期间同步监测空腹血糖、血脂等指标,以评估模型状态。
B6小鼠中约25%个体对高脂饮食不敏感,造模时建议预留25%的富余数量。
3. 饲养管理要点
饲料管理
使用脂肪含量45%–60%的专用DIO饲料,密封防潮,每周更换2–3次。
对照组普通饲料同步更换,保证新鲜度。
垫料选择
避免使用玉米芯垫料,防止小鼠啃食后产生虚假饱腹感,影响高脂饲料摄入。
推荐使用刨花垫料。
操作与护理
抓取操作应温和,避免小鼠挣扎或摔倒。
高脂饲料质地较软,笼内放置硬纸板或小木块供磨牙,防止牙齿过长影响进食。
增加造窝纸,缓解毛发油腻。
定期清洁笼具,清理皮肤褶皱处的饲料碎屑。
FAQ
Q:BKS-DB是否适用于减重药物效果评估?
A:不适用。减重药物在BKS-DB小鼠中通常仅能缓解体重增长趋势。减重评估推荐使用DIO小鼠或B6-Alms1-del模型。
Q:摄食量与摄水量如何检测?
A:检测前更换垫料,称取新饲料并替换原饲料。24小时后,称取剩余饲料及笼内掉落的大块饲料重量,二者差值即为该笼小鼠总摄食量,除以小鼠数量得单只平均摄食量。摄水量检测方法类似。
Q:BKS-DB小鼠血糖超出检测上限时应如何处理?
A:可采用眼眶或颌下取血(约30 µL),分离血浆后稀释,使用血生化仪检测。需注意血生化测得的血糖值与真实值存在差异。该方法因涉及创伤,检测间隔建议为2周,且不适用于GTT检测。可增加糖化血红蛋白检测以反映血糖水平。

