代谢疾病,正在成为小核酸药物的第二增长曲线
小核酸药物正从罕见病适应症拓展至慢性代谢疾病领域。其技术体系已实现关键跃迁:递送技术、化学修饰与临床路径的逐步成熟,使应用方向从罕见病延伸至慢性病,从单一指标控制转向代谢系统重塑。
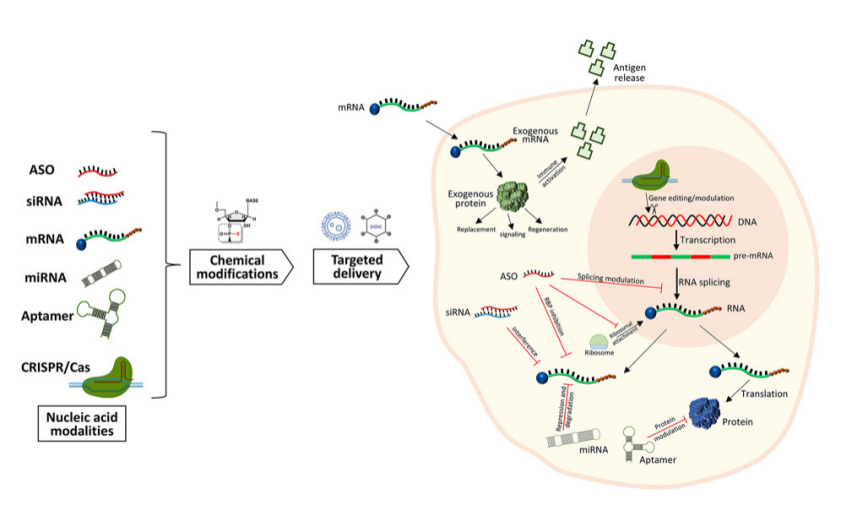
图1. 小核酸药物递送与作用机制
代谢疾病与小核酸药物的契合点
代谢类疾病具备以下与小核酸药物特性高度匹配的共性:
疾病进展缓慢,适合长效、低频给药方案
关键通路由少数枢纽基因主导,靶点逻辑清晰
疗效终点客观可量化,转化路径明确
多数靶点集中于肝脏及代谢相关组织,递送过程更可控
上述特征使小核酸药物能够从基因层面调控代谢通路[2]。
研发重点:能量代谢
能量代谢失衡是肥胖、胰岛素抵抗和代谢综合征的共同底层驱动因素,涉及脂肪、肝脏、肌肉等多组织协同调控。ACVR1C(ALK7)因在脂肪组织中的关键作用,以及与脂肪储存、动员和能量代谢适应的紧密关联,成为小核酸代谢研发中的代表性靶点之一[3]。
案例:ACVR1C靶点人源化模型验证及药效测试
表达验证
人源ACVR1C在B6-hACVR1C小鼠的白色脂肪组织、棕色脂肪组织和附睾白色脂肪组织中成功表达
鼠源Acvr1c不表达
对照:C57BL/6J(n=6,雌性,6-8周龄)
实验组:B6-hACVR1C KI/KI(n=6,3雌3雄,6-8周龄)
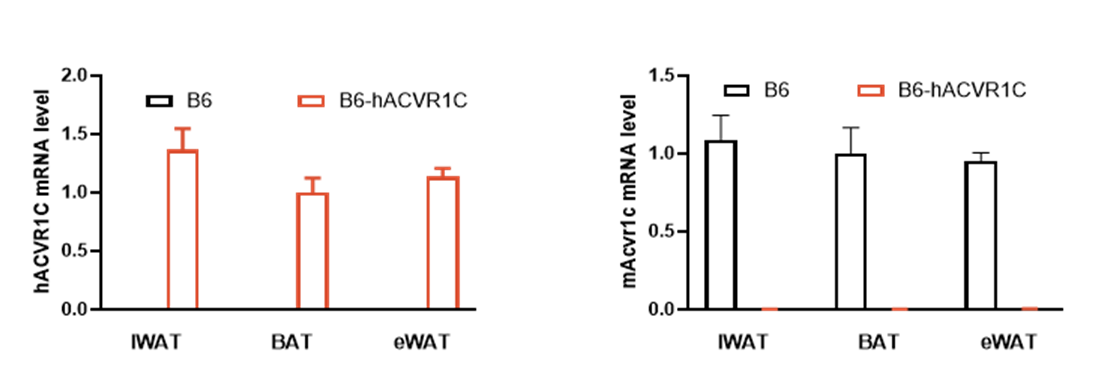
图2. B6-hACVR1C小鼠中人源ACVR1C表达的检测分析
敲低效率检测
模型:B6-hACVR1C小鼠
给药方案:siRNA单次给药
检测时间点:给药后14天终末时间点
实验组:B6-hACVR1C KI/KI基因型小鼠(每组7-8只,雄性)
数据呈现:平均值±标准误(mean ± SEM)
结果:靶向ACVR1C的siRNA可有效降低高脂饮食(HFD)诱导的小鼠体重增长
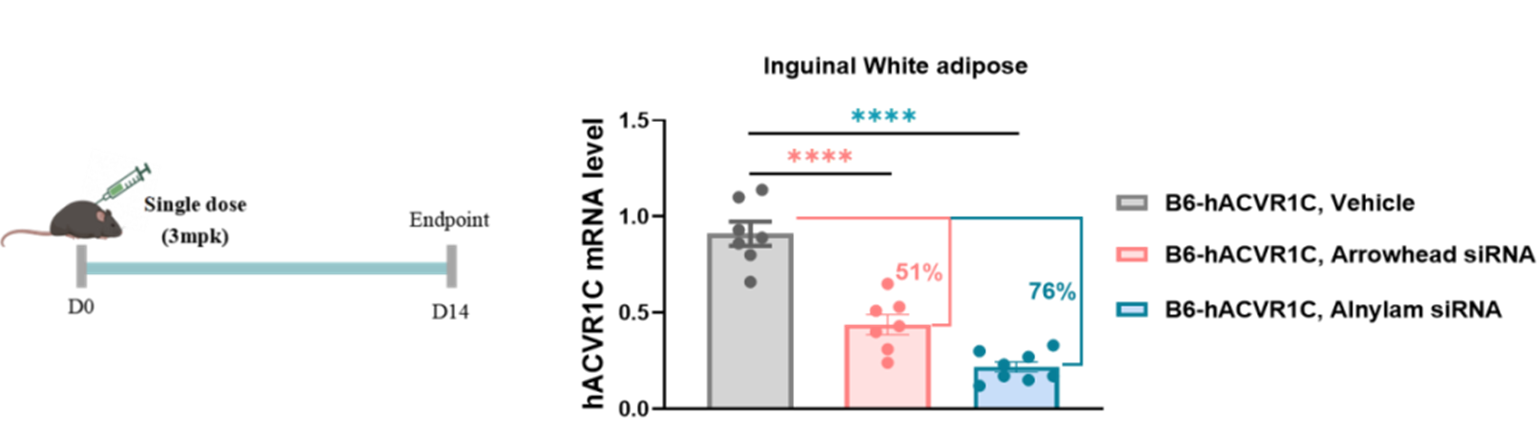
图3. ALK7-siRNA在B6-hACVR1C小鼠中的基因敲低效率研究
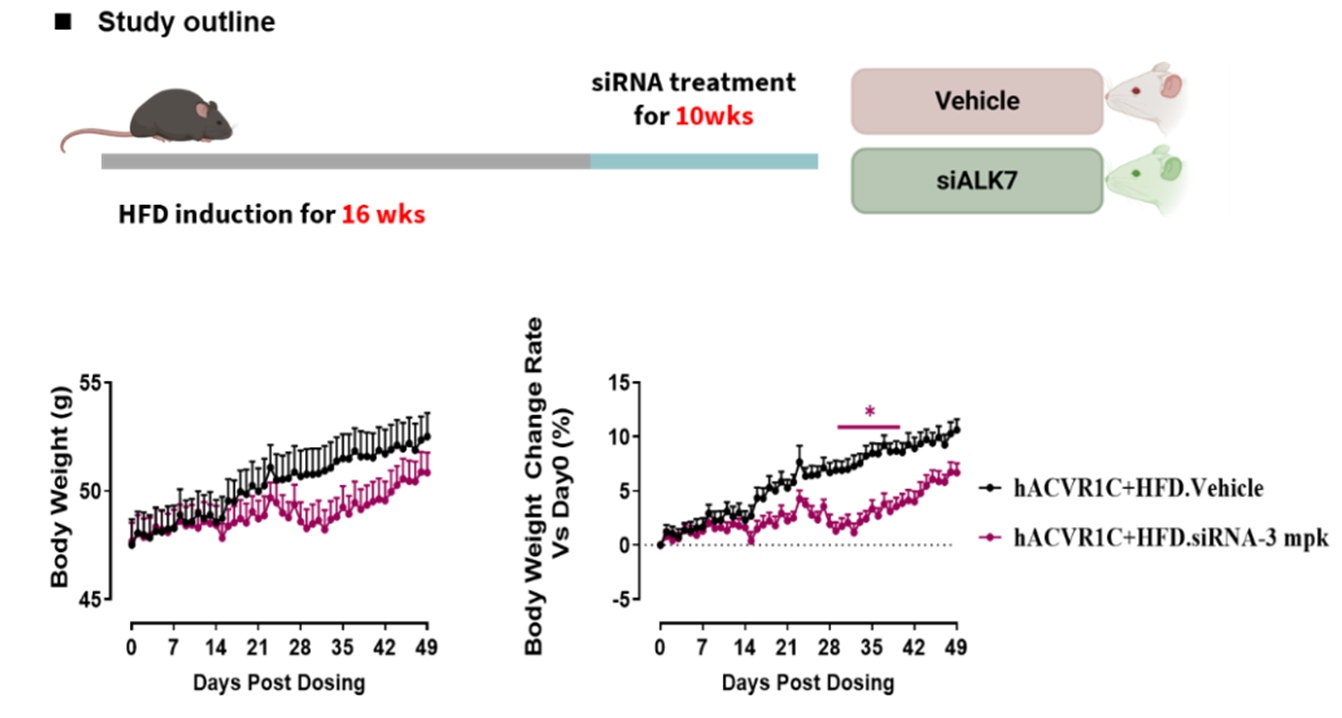
图4. ALK7-siRNA处理B6-hACVR1C小鼠在高脂饮食诱导期间的体重变化
药康生物相关模型资源
药康生物围绕能量调控、脂质代谢及TGF-β家族信号轴,构建了一系列适用于小核酸药物研发的人源化与转基因小鼠模型。具体模型信息可咨询获取。
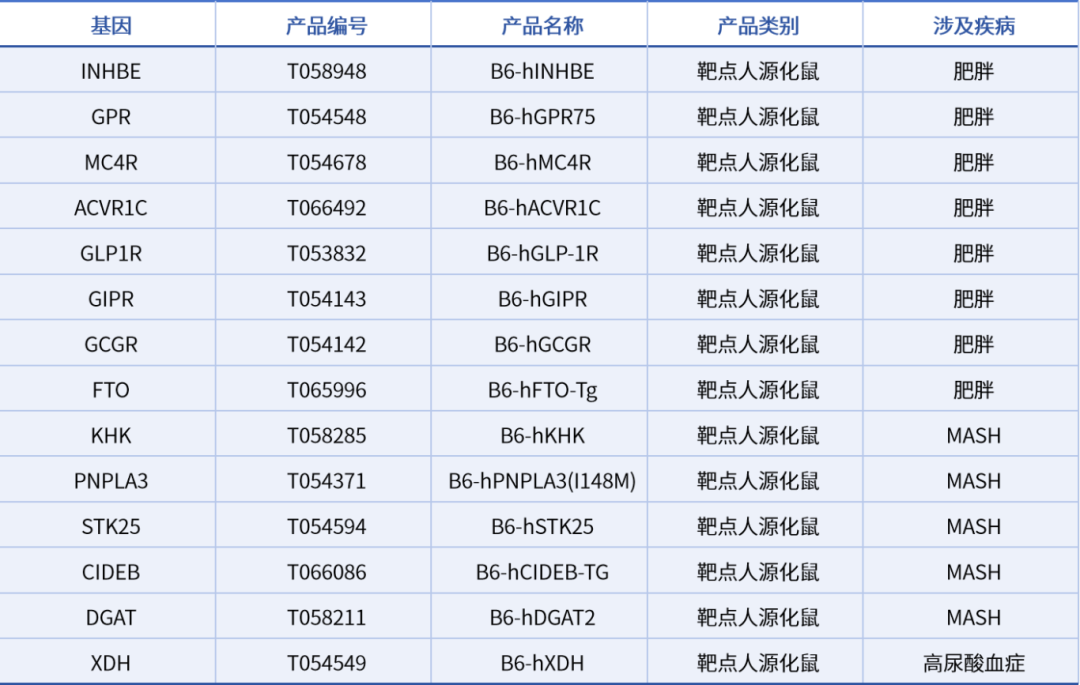
表1. 相关模型列表

