Nature重磅研究:KLHL6为T细胞耗竭提供全新理论靶点与治疗策略
2026 年 1 月 14 日,中国医学科学院系统医学研究院 / 苏州系统医学研究所李贵登团队与 Fred Hutchinson 癌症研究中心 Philip D. Greenberg 团队合作,在Nature与Immunity & Inflammation同步发表两项研究,揭示E3 泛素连接酶 KLHL6为 T 细胞耗竭关键调控靶点,为肿瘤免疫治疗提供全新策略。


一、研究核心背景
T 细胞耗竭是过继性细胞治疗(ACT)抵抗、免疫检查点抑制剂(ICB)耐药的重要原因。
持续、反复的 TCR 信号驱动 CD8+ T 细胞走向功能耗竭,但其核心分子机制尚不明确。
二、关键科学发现
1. 核心调控轴:FOXO1‑KLHL6
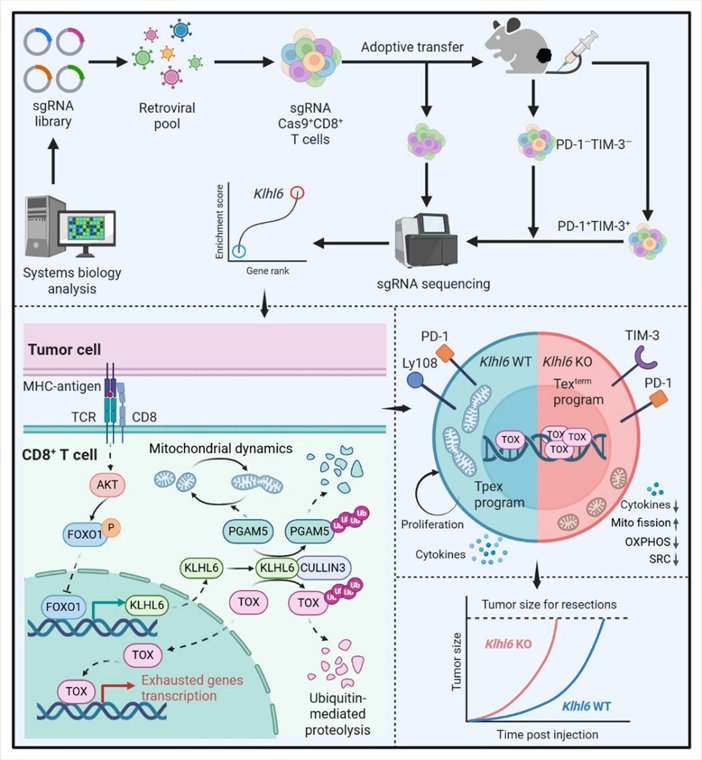
持续 TCR 信号抑制FOXO1转录活性,导致KLHL6持续下调,是驱动 T 细胞耗竭的关键开关。
短暂 TCR 刺激仅暂时抑制 KLHL6,表达可恢复;持续刺激则长期低表达,启动耗竭程序。
2. KLHL6 的作用机制
降解TOX:阻断耗竭核心程序启动,避免终末耗竭分化。
降解PGAM5:维持线粒体稳态,防止过度分裂与呼吸功能损伤,避免代谢紊乱加剧耗竭。
3. 功能验证结果
增强 KLHL6 表达可提升 CD8+ T 细胞抗肿瘤、抗病毒能力,改善线粒体功能,延长荷瘤小鼠生存期。
KLHL6 过表达可提高Tpex比例与数量,降低Texterm比例,阻止 Tpex 向终末耗竭分化,维持持久抗肿瘤免疫应答。
三、药康生物 NCG 小鼠的支撑作用
研究团队采用药康生物 **NCG 小鼠(品系编号:T001475)** 构建人源化肝癌移植瘤模型。
有效验证KLHL6 可显著提升 TCR‑T 细胞在肿瘤微环境中的浸润、存活与功能持久性,为临床前评价提供可靠模型支撑。
四、研究意义与应用前景
从蛋白稳态与泛素化调控维度,阐明持续 TCR 信号驱动 T 细胞耗竭的核心机制。
为靶向TOX/PGAM5的蛋白降解策略、增强 KLHL6 活性的小分子筛选提供理论靶点。
助力CAR‑T、TCR‑T等细胞免疫治疗突破 T 细胞耗竭瓶颈,推动临床转化与创新。

