IF: 88.5! 国产CAR-NK疗法登《柳叶刀》:系统性红斑狼疮治疗实现安全突破
系统性红斑狼疮(SLE)是一种慢性多系统自身免疫疾病,以自身抗体产生、免疫复合物沉积和慢性炎症为特征,影响皮肤、关节、肾脏等多个器官。尽管过去十年中生物制剂如贝利尤单抗、泰它西普等改善了SLE治疗,但仍有部分患者对现有疗法响应不佳,亟需创新治疗策略。近年来,细胞免疫疗法成为SLE治疗的新希望,尤其是靶向致病性B细胞的嵌合抗原受体(CAR)技术。
本研究由海军军医大学长海医院赵东宝教授、高洁副教授、杨建民教授,北京协和医院李梦涛教授,上海长海医院于奕奕博士、孔瑞娜博士及恩瑞恺诺CSO孙明等专家团队共同完成。该团队在国际顶尖医学期刊《The Lancet》上发表了题为"Efficacy and safety of allogeneic CD19 CAR NK-cell therapy in systemic lupus erythematosus: a case series in China"的研究论文。这是同种异体CAR-NK细胞疗法在系统性红斑狼疮中的首个人体临床研究(First in Human),为自身免疫疾病治疗开辟了新方向。
研究背景与意义
SLE的发病机制与B细胞异常活化密切相关,靶向B细胞成为治疗核心。传统疗法如抗CD20单抗(如利妥昔单抗)虽能耗竭外周B细胞,但对淋巴组织和浆细胞效果有限,导致疗效不佳。自体CAR-T细胞疗法通过深度清除CD19+ B细胞,在SLE中实现长期缓解,但其生产耗时、毒性风险高且成本昂贵,限制了广泛应用。
NK细胞作为先天免疫效应细胞,具有直接细胞毒性、低细胞因子分泌特性,且异体应用无需基因编辑即可避免GvHD,为自身免疫疾病提供了更安全、可扩展的解决方案。本研究首次在人体中探索同种异体CAR-NK疗法,旨在解决CAR-T的局限性,推动SLE治疗范式转变。
研究方法
研究设计与参与者
本研究为开放标签、单臂、前瞻性、首次人体病例系列研究,在中国单一中心开展。研究纳入18-65岁复发或难治性SLE成人患者,所有患者既往接受过至少两种标准全身治疗(包括生物制剂如贝利尤单抗或泰它西普),且疾病活动度中度至重度(SLEDAI-2K评分≥8)。患者需满足糖皮质激素依赖或治疗失败标准。研究通过伦理委员会批准,并在ClinicalTrials.gov注册(NCT06010472)。最终纳入18例患者(女性占94%),中位年龄37.5岁,中位病程10.5年,基线SLEDAI-2K评分8-28分,涉及皮肤、肾脏、关节等多器官受累。
干预措施与评估
CAR-NK细胞由健康供者脐带血或外周血NK细胞经基因工程改造制备,靶向CD19,并由恩瑞恺诺公司开发。患者先接受淋巴细胞清除预处理(氟达拉滨25 mg/m²/天+环磷酰胺300 mg/m²/天,第-5至-3天),随后在同一治疗周期内接受三次CAR-NK细胞输注,剂量递增从0.75×10^9细胞开始(剂量水平1-4)。输注间隔根据淋巴细胞恢复情况调整(7天、5天或3天)。
主要终点为安全性和耐受性,包括剂量限制性毒性(DLT)、不良事件(按CTCAE v5.0标准)、细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)。次要终点包括疗效指标:SLE应答指数(SRI-4、SRI-6、SRI-8)、狼疮低疾病活动状态(LLDAS)和DORIS缓解标准。随访时间中位12个月,最长18个月。
研究结果
安全性及耐受性:卓越的安全谱
研究显示,同种异体CAR-NK疗法安全性良好。18例患者中,仅1例(6%)出现1级CRS(发热,自发缓解),未观察到神经毒性、剂量限制性毒性或其他严重不良事件。长期随访(中位11个月)无疾病复发或治疗相关不良事件。与CAR-T疗法相比,CAR-NK细胞未引发显著血细胞减少或感染风险,所有患者IgG水平维持正常(>5 g/L),无需免疫球蛋白替代治疗。下图展示了安全性相关参数:IL-6浓度无显著升高,白细胞和血小板计数稳定,证实了CAR-NK细胞的低毒性特征。
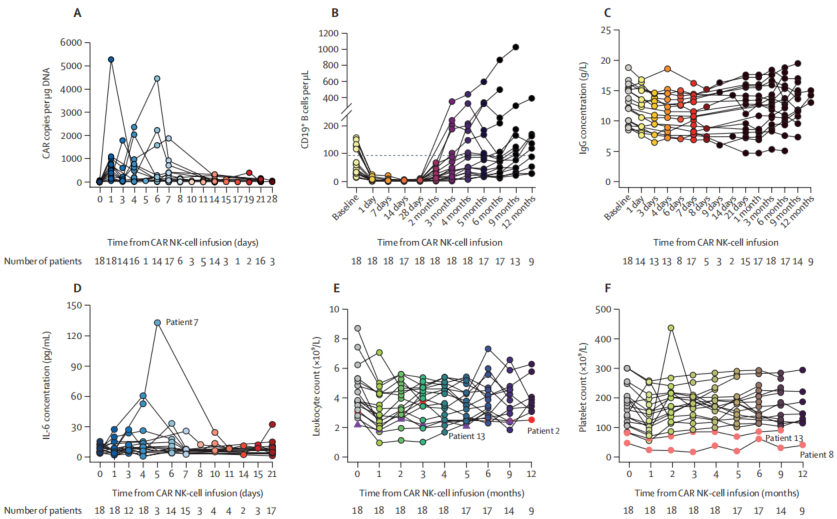
CAR NK细胞疗法的药代动力学、药效学及安全性特征
临床疗效:深度且持久的缓解
自2023年8月21日至2024年6月16日,研究团队在约10个月内成功入组18例中重度复发或难治性系统性红斑狼疮患者,中位随访时间超过12个月,最长随访达18个月;在完成1年以上随访的9例患者中,6例(67%)实现完全DORIS缓解并达到狼疮低疾病活动状态,且无一例复发,同时患者治疗后精神状态、生活质量及工作能力均显著改善,显示出NK细胞疗法的多重获益。安全性方面,18例患者中仅1例(6%)出现1级细胞因子释放综合征,未观察到神经毒性或其他治疗相关严重不良事件,也无剂量限制性毒性发生。进一步通过BCR测序与流式细胞技术分析证实,CAR-NK治疗在绝大多数患者中成功引导了B细胞的免疫重建,为长期深度缓解奠定了机制基础。
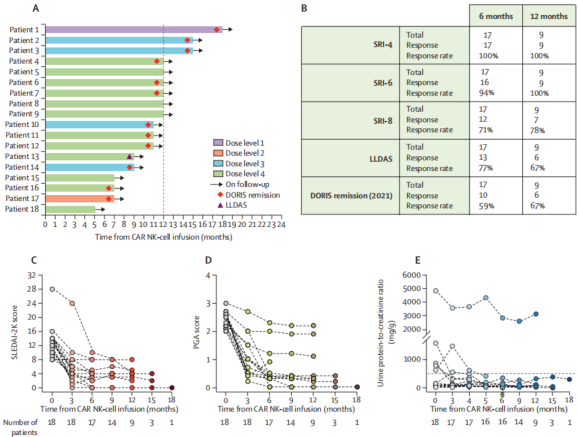
同种异体CD19 CAR-NK细胞疗法的临床疗效
药代动力学与B细胞重建
药代动力学分析显示,CAR-NK细胞在体内短暂存在,峰值浓度出现在输注后第1天(33%患者)、第3-4天(39%)或第7天(28%),14天内逐渐清除,与NK细胞有限寿命一致。尽管持久性短,疗法仍有效耗竭B细胞:89%患者外周血CD19+B细胞降至检测限以下。B细胞重建呈现两种模式:67%患者在2个月内早期恢复,其余在3-4个月延迟恢复,中位恢复时间3个月。重建以幼稚B细胞为主(占比高达96%),记忆B细胞和浆细胞显著减少。免疫球蛋白水平稳定,无患者需要替代治疗,减少了感染风险。
免疫学机制探讨
BCR测序揭示了免疫重置机制。治疗后,71%患者B细胞受体重链分布从IgG/IgA优势转为IgD/IgM,表明同种型类别转换逆转。克隆结构分析显示优势克隆收缩和多克隆受体库(repertoire) 扩张。这种变化说明CAR-NK细胞通过清除自身反应性B细胞克隆,实现双重目标:立即耗竭记忆B细胞库破坏致病cascade,并通过幼稚B细胞再生重建免疫耐受。与CAR-T细胞相比,CAR-NK细胞细胞因子分泌能力较弱,但保留先天抗菌功能,贡献了安全性优势。
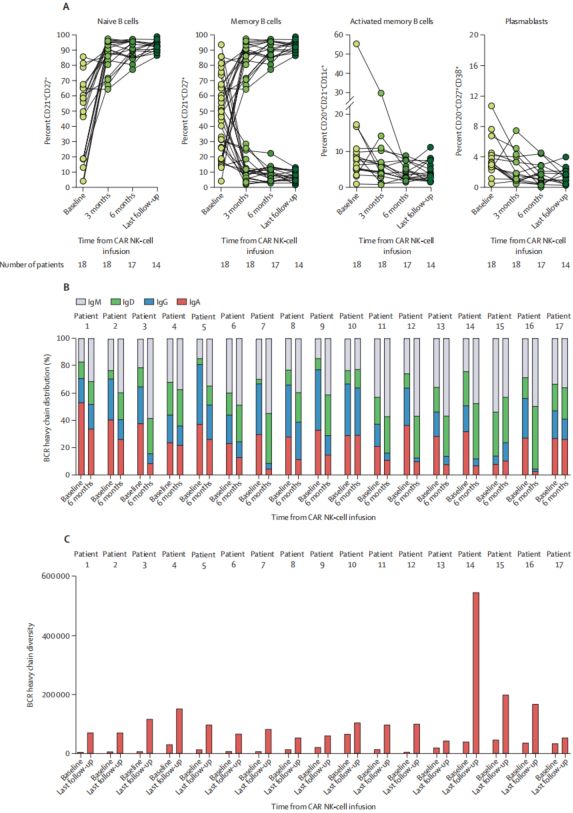
CD19 CAR-NK细胞治疗后B细胞的重建及BCR重链分布与多样性分析
临床意义与创新点
本研究作为首个人体试验,验证了同种异体CAR-NK疗法在SLE治疗中的潜力。其“现货型”特性克服了CAR-T疗法生产复杂、成本高和安全性差的局限,为复发难治患者提供了新选择。疗效的持久性(中位11个月无复发)表明,通过B细胞深度耗竭和重建可能实现长期缓解。免疫学机制上,幼稚B细胞主导的重建和克隆多样性扩张支持了免疫重置假说。
集萃药康致力于提供临床前药效评价解决方案。公司基于自主知识产权的疾病模型小鼠、重度免疫缺陷鼠NCG及其衍生品系,构建了全面的细胞治疗临床前自身免疫疾病药理药效评价平台。该平台覆盖体外和体内研究,拥有丰富的自发疾病模型、诱导疾病模型及免疫重建模型资源,能够满足药物开发的个性化需求,为CAR-NK这类创新疗法的研发提供了坚实的技术支撑。
*本文使用的图片均来自原文献,点击文末“阅读原文”可查看


