17款上市、年销百亿!ADC药物研发最全靶点解析
抗体偶联药物(ADC)正引领肿瘤治疗革命,截至2025年3月,全球获批上市的ADC药物已有17款,2024年度总销售额突破百亿美元。根据Frost&Sullivan的市场分析,到2030年全球市场规模有望增长至647亿美元。作为兼具抗体靶向性与小分子毒性的“智能导弹”,ADC药物疗效的核心在于肿瘤特异性靶点的精准识别。
ADC的结构及原理
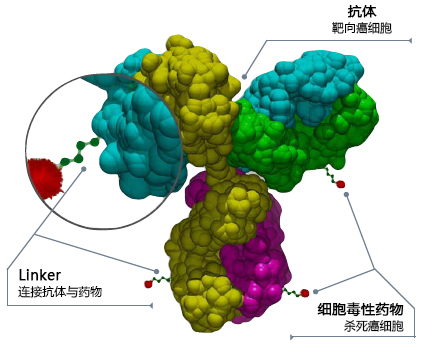
ADC结构[1]
ADC由抗体、连接链和细胞毒性药物三部分组成,通过“四步法”实现精准肿瘤打击:
靶向结合:抗体与肿瘤细胞表面特异性抗原结合,形成ADC-抗原复合物。
内吞转运:复合物通过受体介导的内吞作用进入肿瘤细胞,形成早期内体,后转运至溶酶体。
药物释放:连接链在溶酶体酸性环境或酶作用下裂解,释放高活性细胞毒性药物。
细胞杀伤:药物通过破坏微管结构或诱导DNA损伤,触发肿瘤细胞凋亡;部分药物可穿透细胞膜,杀伤邻近肿瘤细胞(“旁观者效应”)。
ADC靶点格局
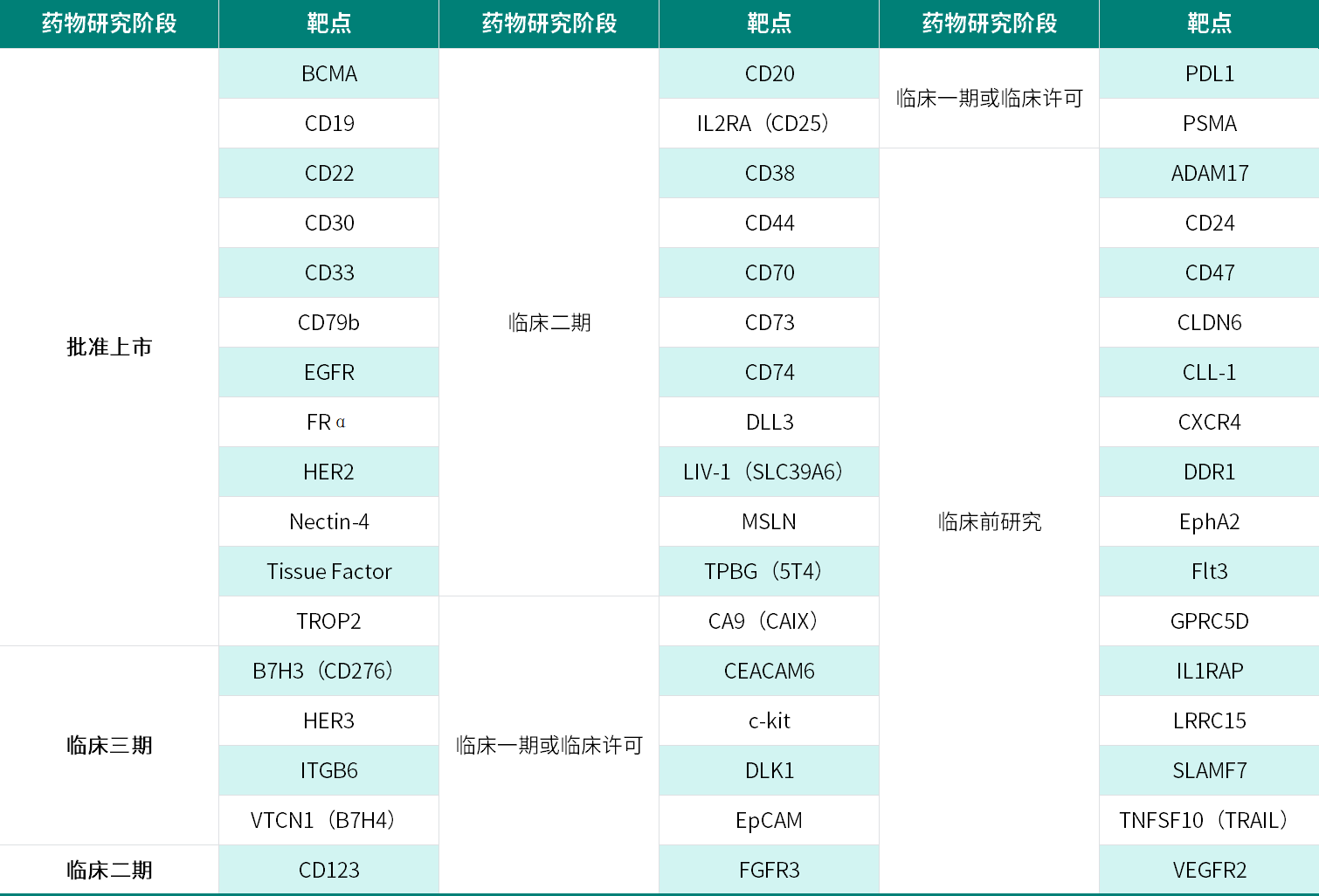
在明确了ADC靶点需满足肿瘤特异性表达、高效内吞及结构稳定等核心标准后,下表进一步梳理了当前全球ADC靶点布局,涵盖已获批上市的成熟靶点(如HER2、Trop-2)及处于不同临床阶段的新型靶点(如B7H3、CLDN6),直观展示了靶点研发的阶段分布与进化趋势。目前17款已上市的ADC药物对应12个靶点,分别为CD33、CD30、HER2、CD22、CD79b、Nectin-4、TROP2、BCMA、EGFR、CD19、Tissue Factor和FRα。
全球ADC研发主要靶点一览[2]
在ADC药物研发中,精准的动物模型是验证药效、评估安全性的关键工具。集萃药康依托其领先的肿瘤模型平台,为ADC药物开发提供了覆盖全流程的模型支持。
ADC药物治疗模型
选用免疫缺陷小鼠接种肿瘤细胞系,进行异种移植物造模,可用于ADC药物的体内药效评价,通过不同抗原表达水平的细胞系验证ADC药物的疗效。集萃药康有BALB/c-Nude、NCG等成熟的免疫缺陷动物模型及衍生品系,并且拥有220+CDX细胞系与200+PDX模型资源库,覆盖胰腺癌、肺癌、胃癌、AML等10种高发及罕见癌种,可用于验证ADC药物作用机制。
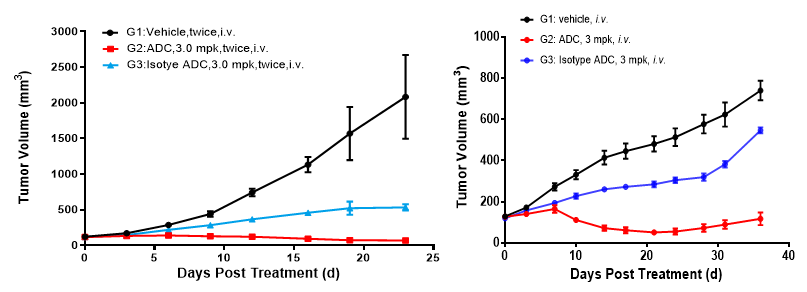
不同模型中ADC药物单药药效评价
(左)BALB/c-Nude+NCI-H1975;(右)NCG+MDA-MB-231
ADC药物与免疫药物联合治疗模型
药物联用也是ADC药物目前研发的重点方向之一,特别是与免疫治疗药物的联合应用:如ADC药物与抗PD-1单抗(Keytruda)联用可以产生双功能PD-1靶向ADC,具有更大的应用前景。
两大核心工具
同系肿瘤模型为肿瘤免疫治疗药物的药效学研究提供了高度仿生的移植瘤资源平台。依托靶点人源化肿瘤细胞系提供精准靶向基础,并结合免疫靶点人源化小鼠模型模拟人体免疫响应,这类模型完整保留了宿主免疫细胞的种类与功能,可精准模拟临床免疫微环境,加速联合方案的转化应用。
免疫重建荷瘤小鼠模型则通过将人源免疫细胞(PBMC或HSC)移植至重度免疫缺陷小鼠(如NCG品系),重建人类免疫系统,从而在小鼠体内模拟人体免疫微环境与肿瘤的相互作用,为ADC与免疫药物的联合治疗提供高度仿真的临床前评价平台。
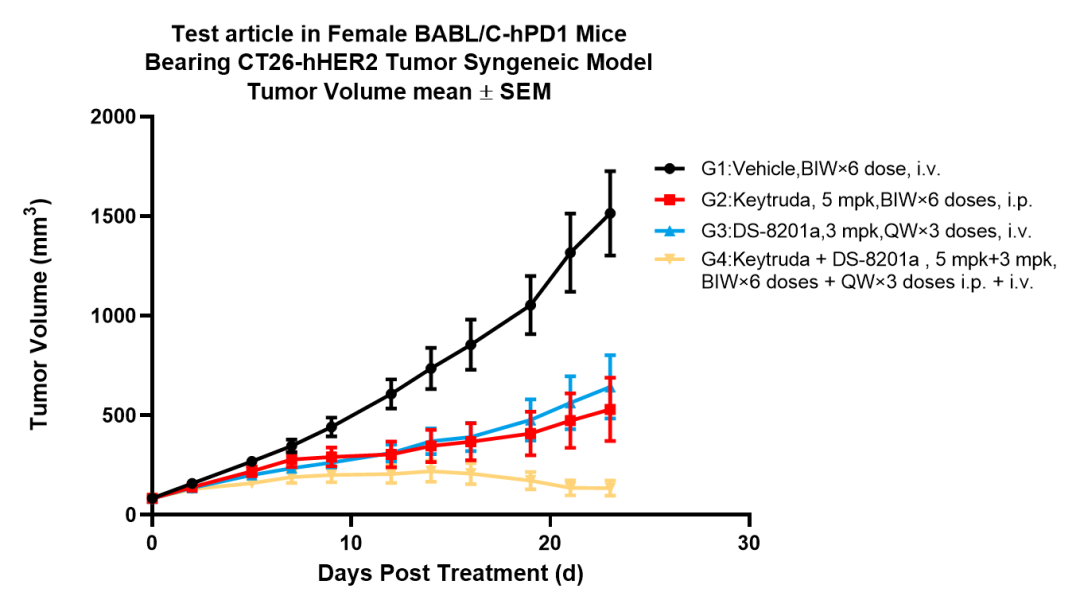
T-DXd与Keytruda联合用药药效评价
ADC药物安全性评价
ADC药物在肿瘤治疗中虽具靶向性强、疗效显著的优势,但其安全性问题需系统验证,涉及多器官毒性风险和机制特异性不良反应。靶点人源化小鼠通过基因编辑技术将免疫健全的小鼠对应靶点替换为人类靶点,可精准模拟人体药物相互作用,为抗体偶联药物(ADC)的抗体部分提供临床前免疫安全性及有效性评估的一体化解决方案,显著提升ADC药物的长毒、生殖毒性等临床前安全性数据的可靠性。
药靶人源化小鼠验证数据
BALB/c-hCD30(T054092)
如图,收集脾脏细胞,经Con A刺激72h后使用流式细胞仪检测。结果发现纯合小鼠T细胞表面只表达hCD30,而野生型小鼠T细胞表面只表达mCD30。
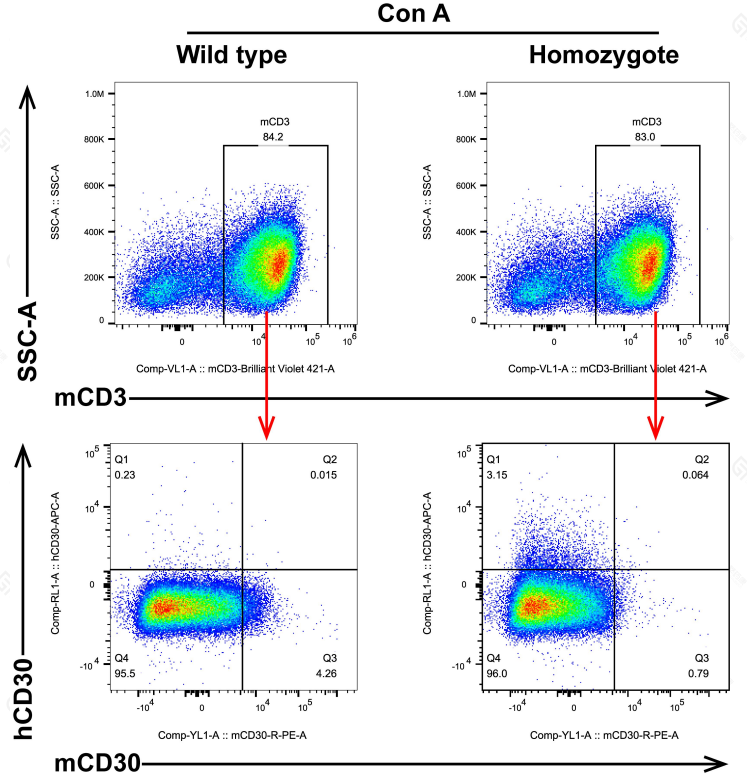
BALB/c-hCD30小鼠hCD30表达检测
集萃药康部分ADC药靶人源化模型列表
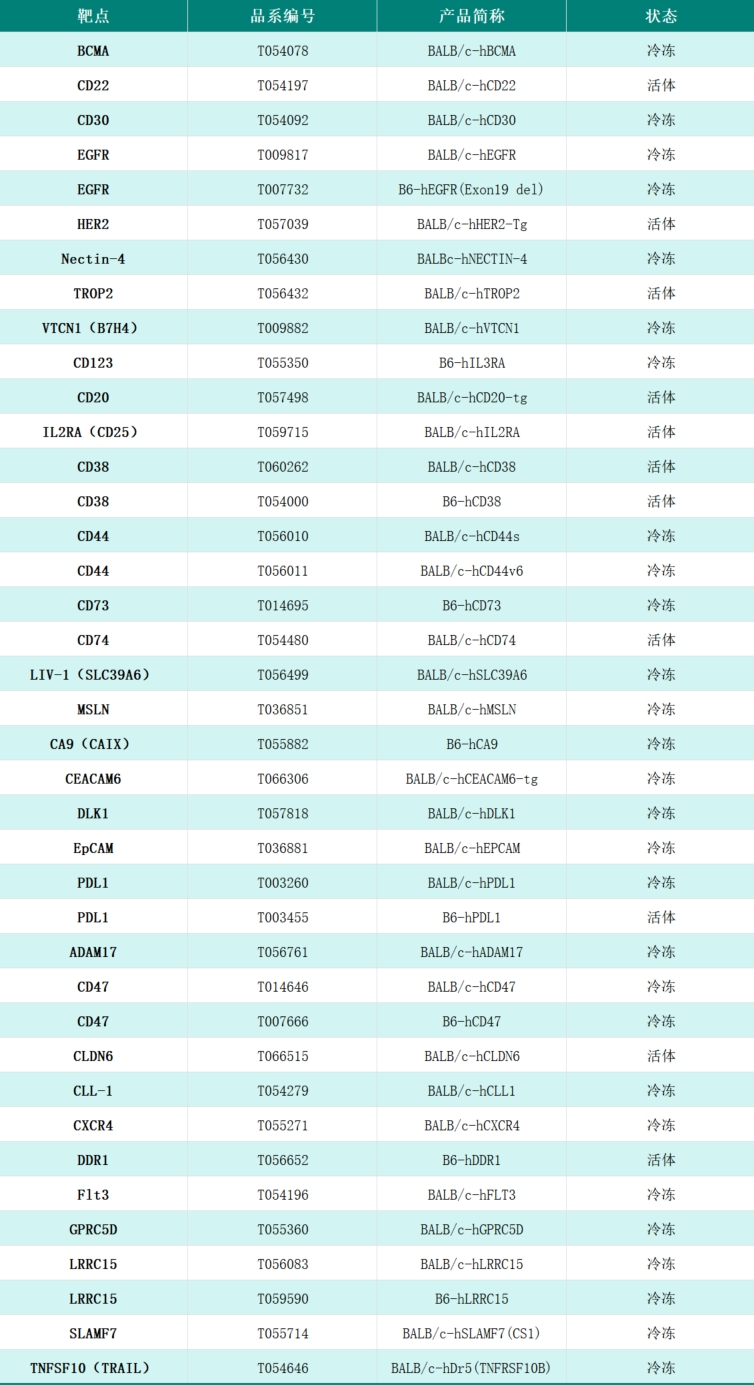
此外,集萃药康还构建了针对ADC payload耐药的肿瘤模型,帮助靶点干预与新型ADC开发。
基于对ADC药物动物模型和其非临床评价的深刻理解,通过“模型+技术+服务”的三维体系,集萃药康为ADC药物开发提供了从实验室到临床前的全方位支持,助力创新药物高效转化。
如想获取更多CDX/PDX等模型数据,欢迎发送邮件至marketing@gempharmatech.com咨询。
参考文献
[1] Signal Transduct Target Ther. 2022, 7(1): 93-117
[2] https://data.pharmacodia.com/domain/#/domainInfo?type=2

