免疫重建升级版来了!NCG-mTslp让淋巴结也"回归"
NCG小鼠是通过基因编辑技术敲除NOD/ShiltJGpt小鼠的Prkdc及Il2rg基因得到的重度免疫缺陷模型。Prkdc基因缺失会阻碍T、B细胞成熟,Il2rg失活会导致NK细胞缺陷,这让NCG模型成为目前免疫缺陷最彻底的小鼠模型之一,是人类肿瘤或免疫细胞移植研究的明星工具。
不过,Il2rg(γc)作为白细胞介素受体的共同亚基,它的缺失会直接阻断IL-7与受体复合物的信号传递。而淋巴组织诱导细胞(LTi 细胞)的发育依赖IL-7信号通路调控,它又是促进淋巴结等次级淋巴组织形成的关键细胞。所以,Il2rg敲除会使得LTi细胞发育受损,导致NCG小鼠淋巴结发育缺陷。淋巴结作为免疫细胞协作的核心枢纽,是B细胞、T细胞等免疫细胞的重要生成、成熟和激活场所。而NCG淋巴结发育缺陷将导致在人造血干细胞移植(HSC)后,影响人源T细胞和B细胞发育及功能。
为进一步提升NCG小鼠HSC重建后免疫细胞功能,集萃药康通过在 NCG 小鼠中过表达胸腺基质淋巴细胞生成素(Tslp),成功实现了淋巴结重塑。TSLP在结构和功能上与IL-7同源,它通过IL-7Rα/TSLPR传递信号,不依赖γc链,过表达Tslp能够恢复与IL-7缺陷相关的淋巴结发育问题,并增强早期B细胞和 T 细胞的淋巴细胞生成。该模型为免疫相关研究及免疫治疗药物筛选提供了有利工具。
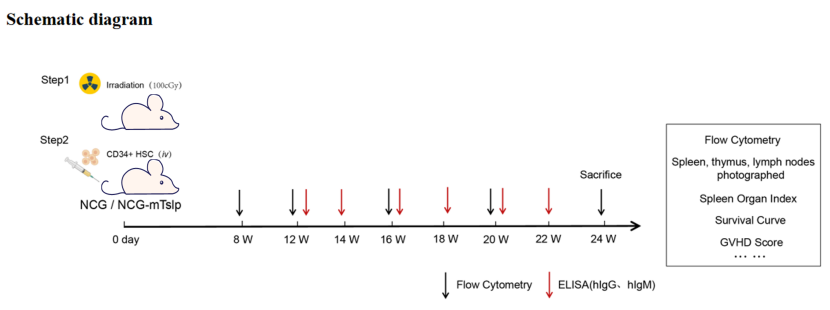
图1. HSC-NCG-mTslp免疫重建流程图
更高的免疫细胞重建水平
收集重建后8~24周龄HSC-NCG、HSC-NCG-mTslp外周抗凝血进行流式检测。流式检测结果显示,与HSC-NCG相比,HSC-NCG-mTslp小鼠外周血中人源CD45+细胞、T细胞、B细胞、NK细胞、未成熟B细胞、过渡B细胞、记忆B细胞和Naive B细胞重建效果优于HSC-NCG小鼠。

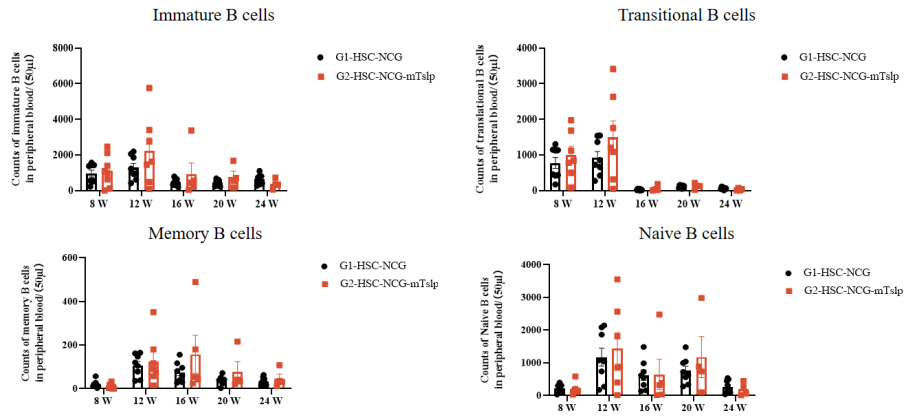
图2. HSC-NCG-mTslp免疫重建结果(n=8)
收集重建后12~24周龄HSC-NCG、HSC-NCG-mTslp血清进行ELISA检测。ELISA结果显示,与HSC-NCG相比,HSC-NCG-mTslp小鼠血清中人源IgG、IgM重建效果优于HSC-NCG小鼠。
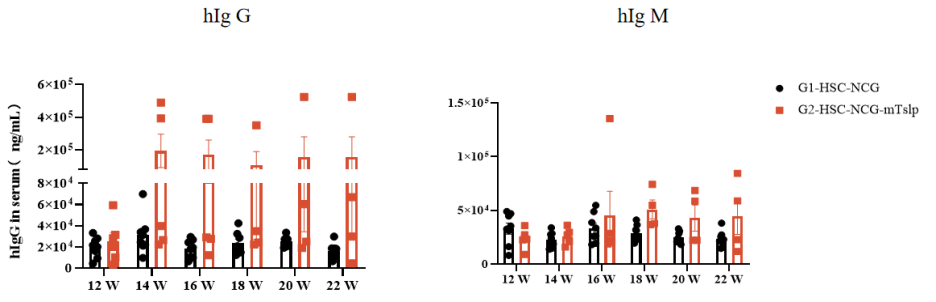
图3. HSC-NCG-mTslp血清中human IgG、IgM ELISA检测结果(n=8)
更高的免疫器官指数
收集重建24周龄HSC-NCG、HSC-NCG-mTslp脾脏称重并计算脏器指数。脾脏指数统计结果显示,与HSC-NCG相比,HSC-NCG-mTslp脾脏指数高于HSC-NCG。
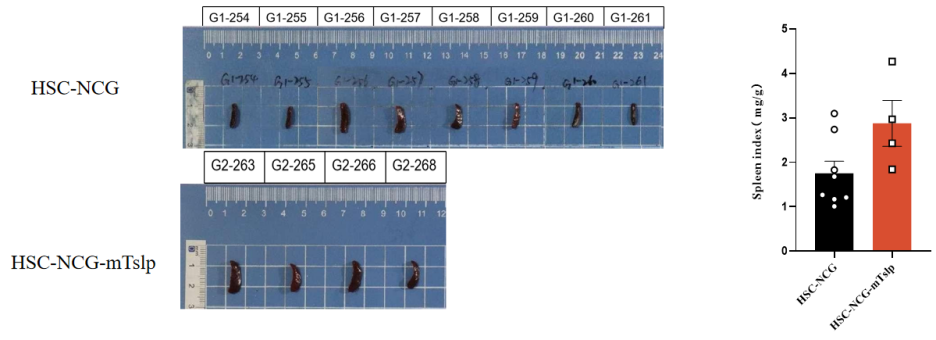
图4. HSC-NCG-mTslp免疫重建24周脾脏指数
收集重建24周龄HSC-NCG、HSC-NCG-mTslp淋巴结并统计数量和大小。结果显示,与HSC-NCG相比,HSC-NCG-mTslp颌下淋巴结、腋下淋巴结、腹股沟淋巴结和肠系膜淋巴结数量和大小显著优于HSC-NCG。
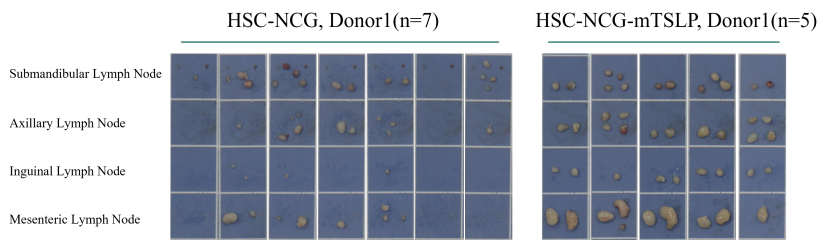
图5. HSC-NCG-mTslp免疫重建24周淋巴结数量和大小统计
HSC-NCG-mTslp小鼠模型的优势
在免疫重建层面,HSC-NCG-mTslp能实现更高水平的免疫细胞重建。流式检测显示,其外周血中的人源CD45+细胞更多,且血清中人源IgG、IgM的重建效果更好。从免疫器官角度来看,HSC-NCG-mTslp的脾脏指数更高,且颌下、腋下、腹股沟和肠系膜等淋巴结更多,表明重建后TSLP的过表达可以显著恢复基因缺陷导致的淋巴结和脾脏发育不良。
作为NCG小鼠的“进阶版”,NCG-mTslp小鼠模型不仅在细胞水平上进行了重建,更首次实现了免疫器官的重塑。该模型可在恶性肿瘤、自身免疫病等领域助力科学家开展药效测试,集萃药康可提供HSC-NCG-mTslp小鼠,赋能相关领域更深入地探索与突破。

