炎症可能诱发癌症?集萃药康小鼠炎症模型助力抗“炎”研究
炎症是一种十分常见而又重要的基本病理过程,任何能够引起组织损伤的因素均可导致炎症的发生。炎症看似是“小病”,但如果控制不当,可能成为某些癌症的诱因。因此,抗“炎”会和免疫、癌症等领域的研究相提并论。为了更准确地观察炎症模型的实验结果,并与人类炎症疾病进行比较研究,集萃药康构建了LPS诱导小鼠炎症模型等丰富品系。
LPS信号转导通路
LPS通过结合宿主细胞表面受体,激活炎性细胞因子基因表达并引起炎症反应,启动细菌的感染过程。LPS进入血流后,首先被血清中的LPS结合蛋白(LPS-binding protein,LBP)识别富集,然后以LPS-LBP复合物的形式与锚定在单核/巨噬细胞、中性粒细胞细胞膜表面的CD14受体分子结合,其后LPS-LBP-CD14三体复合物与TLR4及其相关因子MD-2(myeloid differential protein-2)相互作用,将信号跨膜传递引发细胞内相关通路(IKK-NF-κB途径、MAPK途径)的激活。
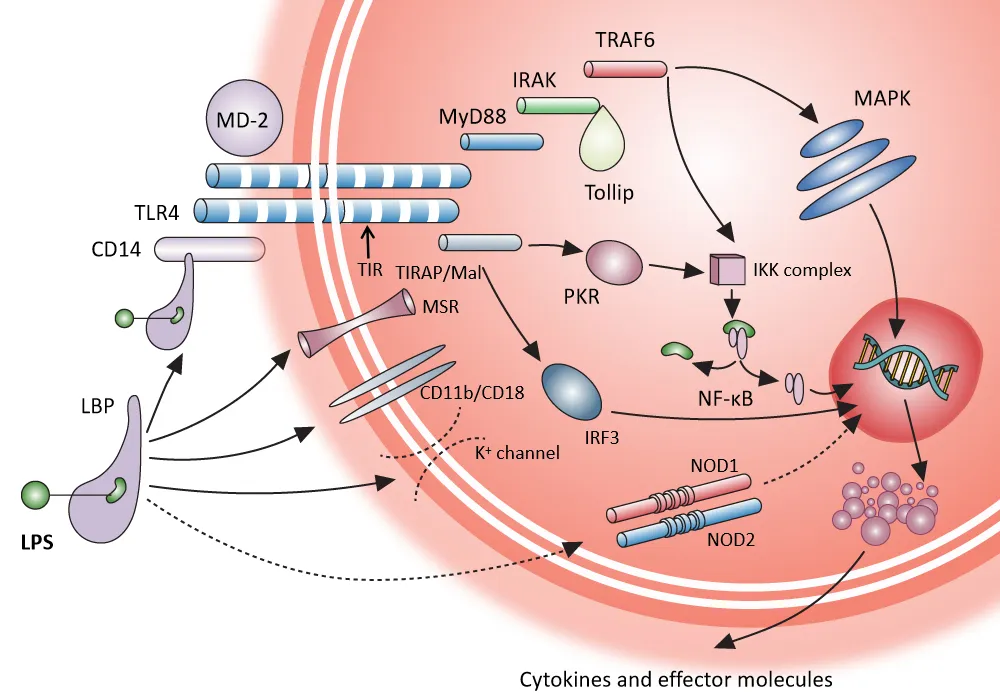
LPS的细胞表面识别机制
集萃药康LPS诱导炎症小鼠模型
LPS是一种常用的刺激剂,可以诱导小鼠炎症模型。集萃药康采用BALB/cJGpt或C57BL/6JGpt小鼠,使用尾静脉注射的方式,成功构建出稳定的小鼠全身炎症模型,并可应用于药物临床前评价。
模型数据
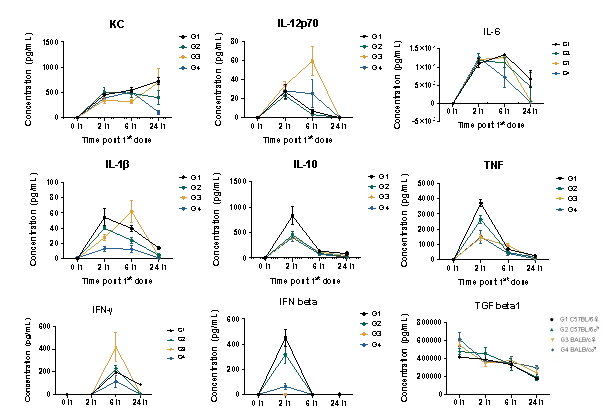
尾静脉注射LPS建立小鼠全身炎症模型。在诱导后0,2,6,24h检测小鼠血液中炎性细胞因子的表达情况。结果显示LPS诱导后炎性细胞因子显著释放,细胞因子浓度在不同时间点达到最大值。
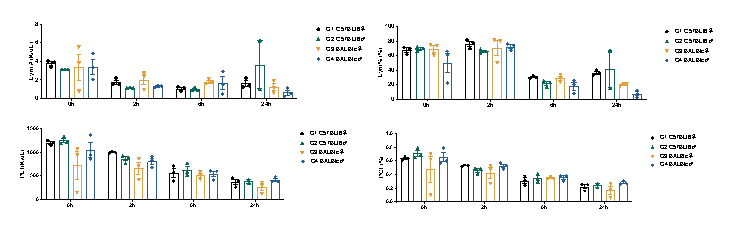
小鼠全血检测结果显示,LPS诱导后淋巴细胞计数和血小板含量下降。
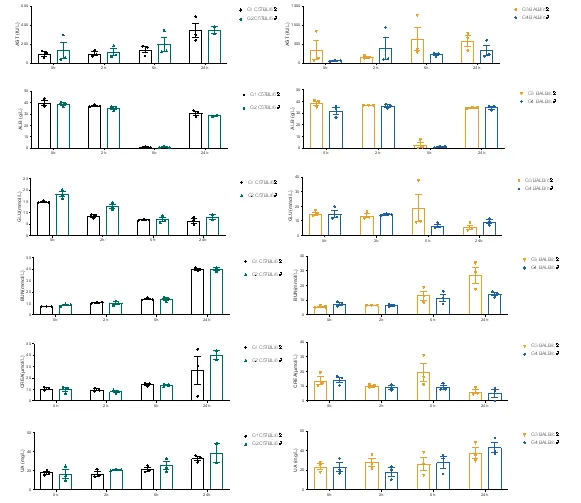
LPS诱导后可观察到严重的肝、肾损伤,并且小鼠血糖水平下降。
(左:G1 C57BL/6♀、G2 C57BL/6♂;右:G3 BALB/c♀、G4 BALB/c♂ )
LPS诱导炎症模型应用于药效评价
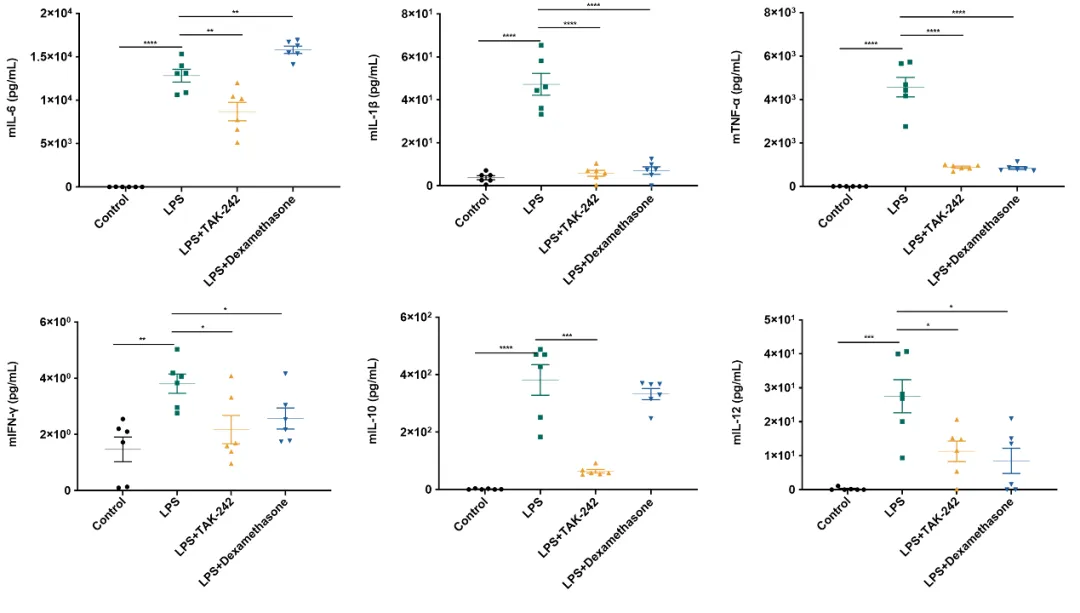
LPS造模前1h给予药物(TAK-242和醋酸地塞米松),LPS造模后2h采集血清检测炎性细胞因子表达。结果显示,TAK-242和醋酸地塞米松给药组能明显抑制LPS诱导的炎性细胞因子表达。
模型应用场景1—药物临床前初步验证
候选药物众多毫无头绪?集萃药康帮你筛!集萃药康LPS诱导小鼠炎症模型具有易于建立、稳定性高、试验周期短的优点,使小鼠的先天免疫反应被激活,高水平的促炎细胞因子被释放,该模型为有效的全身炎症模型,可用于确定被试化合物的抗炎潜力。
模型应用场景2—炎症性疾病模型
脓毒症(Sepsis)是由细菌等病原微生物侵入机体引起的全身炎症反应综合征。主要表现为寒战、发热(或低体温)、心慌、气促、精神状态改变等症状。脓毒症可发展为严重脓毒症和脓毒性休克,可导致器官功能不全及循环障碍,是严重创伤、烧伤、休克、感染和外科大手术等常见的并发症,病死率较高。脓毒症及其相关并发症仍旧是当今急危重症医学面临的突出难题。
集萃药康LPS诱导的炎症小鼠模型可很好的模拟脓毒症的发病机理,并表现出相应表型,可作为脓毒症小鼠模型使用,并用于脓毒症药物临床前评价。
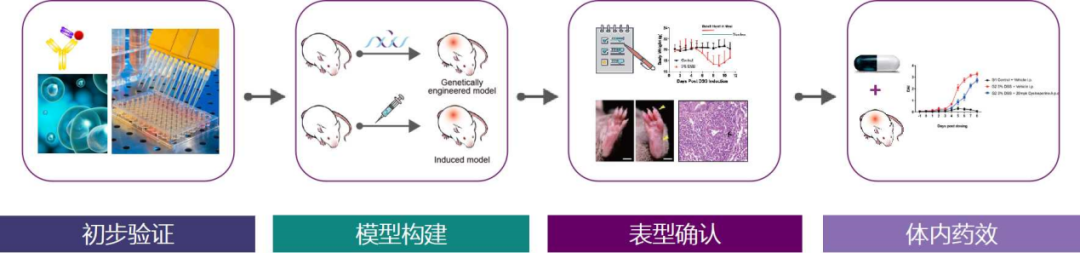
集萃药康自免平台可提供动物模型和技术服务,并可定制药物开发临床前一站式服务,主要聚焦系统性红斑狼疮、炎性肠病、多发性硬化症、银屑病、特应性皮炎、类风湿性关节炎、特发性肺纤维化等疾病领域。
自免临床前一站式服务